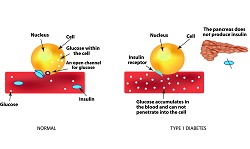
Ri-educazione del sistema immunitario per combattere il diabete
Attualmente ci sono oltre mezzo milione di malati di diabete di tipo 1 in Europa, una malattia per la quale non ci sono cure né metodi di prevenzione. La distruzione delle cellule beta produttrici di insulina è un processo graduale e la maggior parte dei pazienti al momento della diagnosi ha ancora un residuo di produzione di insulina. I risultati del Diabetes Control and Complications Trial (DCCT) hanno indicato che gli individui che hanno un residuo di insulina hanno un migliore controllo glicemico, un tasso ridotto di ipoglicemia e un rischio più basso di complicazioni a lungo termine. La maggior parte dei metodi di cura sono progettati per sostituire in modo efficiente i livelli di insulina bassi o assenti nei pazienti. Il basso tasso di efficienza di questa strategia però suggerisce che la conservazione di quantità anche piccole di produzione endogena di insulina potrebbe costituire un’alternativa per migliorare il controllo glicemico. Questo non solo ridurrà l’ipoglicemia ma anche le complicazioni a lungo termine come i problemi alla vista, l’insufficienza renale e le ulcere diabetiche. Gli scienziati del progetto EE-ASI, finanziato dall’UE, hanno proposto un approccio di immunoterapia specifica antigene epidermica potenziata (EE-ASI) per ri-educare il sistema immunitario perché smetta di distruggere le cellule beta pancreatiche. Questo sistema innovativo somministra peptidi presenti solo sulle cellule beta in nanoparticelle d’oro. Come spiega il coordinatore del progetto, il prof. Dayan, “Le nanoparticelle sono assorbite in modo efficiente dalle cellule dendritiche portando alla presentazione del peptide in un contesto non-infiammatorio, che promuove la generazione di cellule T regolatrici.” Un secondo carico tolerogenico come l’Interleuchina-10, oltre all’antigene, è incluso per promuovere la produzione di cellule T regolatrici. Distribuzione di nanoparticelle Anche se il metodo EE-ASI assomiglia alla vaccinazione, il suo obiettivo è disattivare le risposte autoimmuni attivando le cellule T regolatrici. Queste riconoscono le proteine del sé e agiscono proattivamente per sopprimere eventuali tentativi del corpo di sviluppare risposte immunitarie alle proteine del sé. Nell’EE-ASI, i partner hanno caricato il peptide proinsulina C19-A3 in nanoparticelle di oro con un’efficienza molto alta. “L’oro è molto inerte e ha proprietà anti-infiammatorie che sembrano essere benefiche,” continua il prof. Dayan. Quando somministrate ex vivo sulla pelle umana con microaghi, queste nanoparticelle piene di peptide si diffondono nell’epidermide e sono assorbite dalle cellule di Langerhans. Per farlo le loro dimensioni devono essere di cinque nanometri di diametro perché le particelle più grandi non seguono questo schema di diffusione. Gli esperimenti pre-clinici sui topi hanno dimostrato una diffusione a linfonodi distanti in modo più rapido rispetto al peptide da solo. Studi di tossicologia hanno verificato la sicurezza di questo approccio e hanno portato alla richiesta di un brevetto e a uno studio clinico di fase I in meno di quattro anni dall’inizio del progetto. Efficacia clinica Lo studio clinico EE-ASI rappresenta il primo studio sull’uomo sugli effetti della somministrazione di un peptide di proinsulina coniugato a nanoparticelle. I risultati hanno rivelato che quando somministrato in forma intradermica, l’oro rimane nella pelle per più di sei mesi insieme a un infiltrato linfocitico locale che richiede ulteriori indagini. Ulteriori studi determineranno anche se il peptide rimane associato all’oro. Inoltre il consorzio sta “studiando altre molecole tolerogeniche e l’incorporazione di molecole di DNA per esprimere peptidi del sé nella pelle,” sottolinea il prof. Dayan. Anche se non ci sono ancora studi di efficacia, incoraggiare il corpo a riconoscere l’insulina e a fermarne la distruzione immunitaria sembra un metodo valido per curare il diabete di tipo 1. Data la facilità di applicazione, il metodo EE-ASI promette una migliore collaborazione da parte del paziente e meno complicazioni rispetto alla terapia di sostituzione dell’ormone. A sua volta questo porterà a migliori esiti clinici e a una migliore qualità della vita per i malati di diabete e le loro famiglie.
Parole chiave
Sistema immunitario, immunoterapia, diabete di tipo 1, insulina, cellule beta pancreatiche, EE-ASI, nanoparticelle, cellule T regolatrici, Interleuchina 10, proinsulina