Un nouveau capteur détecte les maladies infectieuses en l’espace de 6 minutes
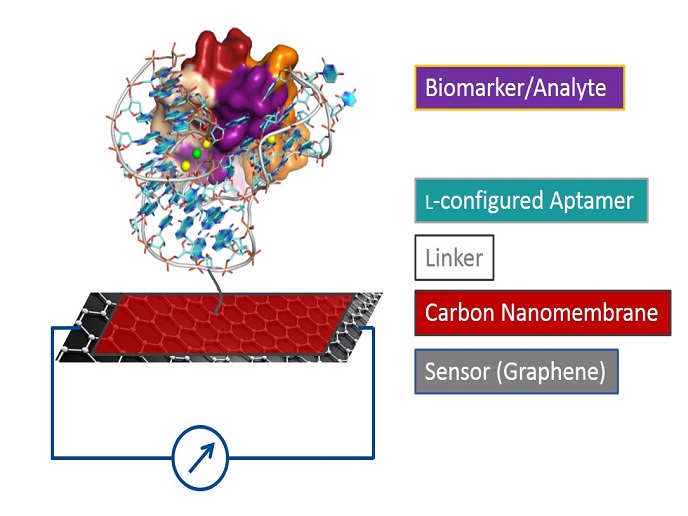
Le projet PoC-ID(s’ouvre dans une nouvelle fenêtre) a mis au point de nouveaux capteurs microélectroniques et les ont intégrés dans un appareil de paillasse de diagnostic in vitro sur le lieu d’intervention (PoC-ID). «La plateforme est porteuse d’espoir pour les patients dans la mesure où elle permet un diagnostic rapide et un traitement approprié, ce qui réduira également les coûts des soins de santé», souligne la Dre Tanja Braun, coordinatrice du projet. Les applications de l’appareil PoC-ID comprennent le diagnostic, le suivi des réponses thérapeutiques, la recherche sur l’interaction agent pathogène-hôte et la médecine personnalisée. De plus, la plateforme peut facilement être adaptée à de nombreuses fins de biodétection, telles que le suivi sanitaire ou environnemental ou les tests de qualité alimentaire. L’équipe du projet a mis au point le prototype PoC révolutionnaire pour le diagnostic de l’infection par le virus respiratoire syncytial (VRS), en particulier chez les enfants. Comparé à la norme actuelle, fondée exclusivement sur la détection d’agents pathogènes, l’appareil utilise une approche de rupture en ce sens qu’il mesure à la fois l’agent pathogène infectieux et la réponse de l’hôte. Cette approche permet de faire la distinction entre les agents pathogènes causatifs pertinents sur le plan clinique et les agents pathogènes présents, mais inoffensifs. Les nouveaux capteurs combinent des nanomembranes et des molécules de capture (L-aptamères) obtenues par génie génétique. L’équipe du projet les a utilisées pour adapter, de manière très spécifique, la réponse d’un transistor à effet de champ en graphène (BioGrFET) et d’un système microélectromécanique (BioMEMS) aux cibles biologiques. Cela a débouché sur le développement de L-aptamères contre trois molécules cibles identifiées, induites dans les sécrétions respiratoires à la suite d’une infection par le VRS. L’un de ces L-aptamères est le facteur de réponse de l’hôte, à savoir l’interleukine 8. Il a été possible d’immobiliser les L-aptamères grâce à l’emploi d’une nanomembrane de carbone (CNM), qui ajuste la réponse d’un BioGrFET ultra-sensible couvrant la gamme d’interleukine 8 la plus pertinente sur le plan clinique. De plus, les travaux du projet se sont axés sur la valeur clinique des marqueurs inflammatoires présents dans l’écouvillonnage du nasopharynx pendant l’infection par le VRS. «Il est important de noter que l’interleukine 8 a été confirmée comme biomarqueur capable de différencier les enfants atteints de maladies modérées et graves, ce qui permet d’identifier les patients nécessitant des soins de soutien dans un hôpital», explique la Dre Braun. Le coût des nouveaux capteurs jetables est faible, car aucun tampon ni enzyme biologiquement actifs et coûteux ne sont nécessaires à des fins de détection. En outre, si ces capteurs sont produits en masse, leurs coûts seront très faibles grâce à la conception du flux de production microélectronique. «L’affichage électronique parallèle permet une détection rapide et multiplexée», souligne la Dre Braun. L’intégration de capteurs, d’un affichage électronique et de la microfluidique dans une plateforme PoC conviviale a permis d’accomplir d’autres progrès en termes d’ergonomie et de rapidité d’analyse des données. Deux demandes internationales de brevet ont été déposées pour l’immobilisation d’oligonucléotides sur des CNM. L’utilisation de CNM revêtues d’aptamères qui présentent une forte adhérence au graphène permet de maintenir les aptamères à la surface du graphène car, à leur défaut, ils ne pourraient pas être fonctionnalisés sans perdre leurs remarquables propriétés électriques, et de préserver l’affinité cible des aptamères. Par ailleurs, une demande de brevet a été déposée pour le L-aptamère liant l’interleukine 8. L’utilisation de cette molécule a permis d’effectuer la validation de principe portant sur la possibilité de détecter une biomolécule avec le capteur BioGrFET à l’aide d’un nano-injecteur CNM. Évoquant uniquement les applications cliniques, la Dre Braun résume l’importance de ce capteur révolutionnaire. «La nouvelle plateforme soutiendra la prévention et le contrôle de la propagation des agents pathogènes et permettra un traitement plus rapide et plus personnalisé pour les patients.»