Neuer Sensor erkennt Infektionskrankheiten in sechs Minuten
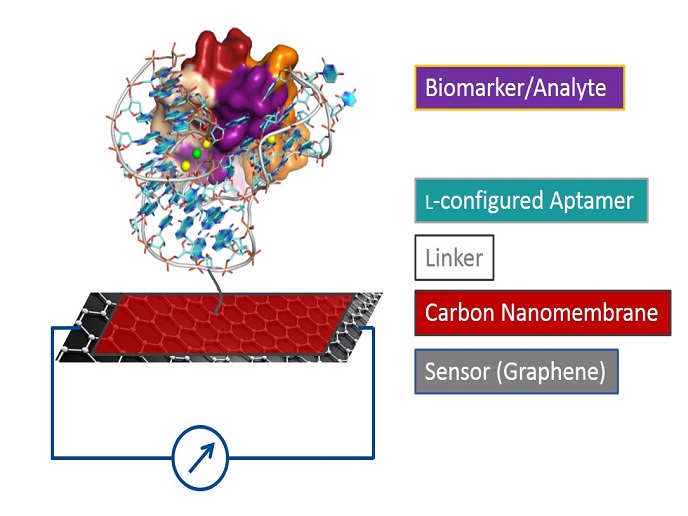
Im Rahmen des Projekts PoC-ID(öffnet in neuem Fenster) wurde neue Mikroelektronik entwickelt, die auf Sensoren in einem patientennahen In-vitro-Diagnose-Tischgerät (PoC-ID) basiert. „Die Plattform verspricht für Patienten von Nutzen zu sein, da sie eine schnelle Diagnose und korrekte Behandlung ermöglicht – hierdurch werden ebenfalls die Gesundheitsversorgungskosten gesenkt“, betont Projektkoordinatorin Dr. Tanja Braun. Zu den Anwendungsbereichen des PoC-ID-Geräts zählen die Diagnose, die Überwachung therapeutischer Reaktionen, die Forschung an Wechselwirkungen zwischen Pathogen und Wirt sowie die personalisierte Medizin. Die Plattform kann zudem ohne Weiteres auf eine Vielzahl an Zwecken im Bereich der Biosensorik angepasst werden, darunter die Gesundheits-/Umweltüberwachung oder Lebensmittelqualitätsprüfungen. Das Projektteam entwickelte den bahnbrechenden PoC-Prototypen für die Diagnose von Respiratorischen Synzytial-Virus-Infektionen (RSV), die vor allem Kinder betreffen. Im Vergleich zur aktuellen Praxis, die ausschließlich auf die Detektion von Pathogenen ausgerichtet ist, verwendet das Gerät einen revolutionären Ansatz, da die Reaktion des infektiösen Pathogens wie auch die Reaktion des Wirts gemessen wird. Dies ermöglicht die Unterscheidung zwischen klinisch relevanten Verursacher-Pathogenen und ggf. vorhanden Pathogenen, die keinen Schaden anrichten. Die neuen Sensoren nutzen eine Kombination aus Nanomembranen und durch Molekulartechnik hergestellten Fängermolekülen (L-Aptamere). Das Projektteam wandte diese zur Herstellung der Reaktion eines Graphen-Feldeffekttransistors (BioGrFET) und eines mikroelektromechanischen Systems (BioMEMS) an, die eine hohe Empfindlichkeit für die biologischen Ziele aufweisen. Es wurden L-Aptamere gegen drei identifizierte Zielmoleküle entwickelt, die nach RSV-Infektionen in Atemwegssekrete induziert werden. Eines ist der Entzündungsmediator Interleukin-8. Die Immobilisierung von L-Aptameren wurde durch eine Kohlenstoffnanomembran (CNM) ermöglicht, welche die Feinabstimmung der Reaktion eines ultraempfindlichen BioGrFET ermöglicht, um das Interleukin-8-Spektrum mit der größten klinischen Relevanz abzudecken. Außerdem wurde der klinische Wert von inflammatorischen Markern untersucht, die während einer RSV-Infektion in einer nasopharyngealen Probe vorhanden sind. „Interleukin-8 wurde als ein Biomarker bestätigt, der zwischen Kindern mit moderater und schwerer Erkrankung unterscheiden kann, um zu bestimmen, wer unterstützende Betreuung in einem Krankenhaus benötigt“, erklärt Dr. Braun. Die Kosten für die neuen Einmal-Sensoren sind gering, da für die Detektion keine kostspieligen biologisch aktiven Puffer oder Enzyme erforderlich sind. Bei hohen Volumen sind die Kosten aufgrund der Mikroelektronik-Fertigung am Fließband außerdem sehr gering. „Die Detektion gestaltet sich aufgrund der parallelen elektrischen Auslese im Multiplexverfahren schnell“, merkt Dr. Braun an. Weitere Fortschritte wurden hinsichtlich der Benutzerfreundlichkeit und Datenanalysegeschwindigkeit erzielt, die aus der Integration von Sensoren, Ausleseelektronik und Mikrofluidik in eine benutzerfreundliche PoC-Plattform resultieren. Es wurden zwei internationale Patentanträge zur Immobilisierung von Oligonukleotiden auf CNM eingereicht. Die Verwendung von Aptamer-beschichteten CNM, die eng an Graphen gebunden sind, ermöglicht es, die Aptamere an der Graphenoberfläche zu halten, die anderenfalls nicht ohne den Verlust ihrer herausragenden elektrischen Eigenschaften funktionalisiert werden könnten, und überdies bleibt die Zielaffinität der Aptamere erhalten. Im Weiteren wurde ein Patentantrag zu dem L-Aptamer eingereicht, das sich an Interleukin-8 bindet. Die Verwendung dieses Moleküls als Konzeptnachweis für die mögliche Detektion eines Biomoleküls mit dem BioGrFET-Sensor unter Anwendung eines CNM-Nanointerposers wurde erfolgreich erreicht. Mit Blick allein auf die klinische Anwendung fasst Dr. Braun die Bedeutung dieses revolutionären Sensors folgendermaßen zusammen. „Die neuartige Plattform wird die Prävention und Kontrolle der Pathogenausbreitung unterstützen und eine schnellere sowie personalisiertere Patientenbehandlung ermöglichen.“