Des protéines fondamentales du cerveau fournissent des indices précoces de la maladie d’Alzheimer
La cause exacte de la maladie d’Alzheimer n’a pas encore été élucidée, mais des recherches récentes montrent que la maladie est identifiée par l’accumulation de deux protéines dans le cerveau appelées amyloïde bêta (Aβ) et tau. Le projet CONNECT, financé avec le soutien des actions Marie Skłodowska-Curie de l’UE, visait: «À identifier les premiers changements cérébraux mesurables qui indiquent l’accumulation de ces protéines. Nous pouvons ensuite utiliser ces informations pour prédire qui est le plus susceptible de progresser ultérieurement vers la maladie d’Alzheimer», explique Heidi Jacobs, professeure adjointe à l’École de santé mentale et de neurosciences de l’Université de Maastricht(s’ouvre dans une nouvelle fenêtre) aux Pays-Bas. Les scientifiques savent désormais que ces protéines s’accumulent dans le cerveau de 20 à 30 ans avant que les premiers symptômes cliniques d’Alzheimer, comme la perte de mémoire, la confusion ou la désorientation, ne commencent à apparaître. Les données d’autopsie montrent que les protéines tau commencent à s’accumuler vers l’âge de 20 ans dans une minuscule région cachée dans le tronc cérébral, connue sous le nom de locus coeruleus, du latin «tache bleue», car ses cellules pigmentées apparaissent en bleu lors de l’autopsie. À mesure que les gens vieillissent, la pathologie tau progresse vers les régions cérébrales essentielles au fonctionnement de la mémoire, explique Heidi Jacobs. D’un autre côté, vers 50-60 ans, les protéines Aβ commencent à s’accumuler, se déplaçant dans la direction opposée. Elles commencent plus haut dans le cortex ou dans les couches externes du cerveau et atteignent le tronc cérébral pendant les stades avancés de la maladie. Les neuroscientifiques pensent que ces deux protéines interagissent, conduisant à des déficits cognitifs détectables, selon Heidi Jacobs. «Les changements dans la tache bleue pourraient présager un déclin cognitif ou la maladie d’Alzheimer, mais en raison de son emplacement, cette tache bleue est difficile à mesurer en utilisant des méthodes d’imagerie classiques», explique-t-elle.
Enquêter sur la «tache bleue»
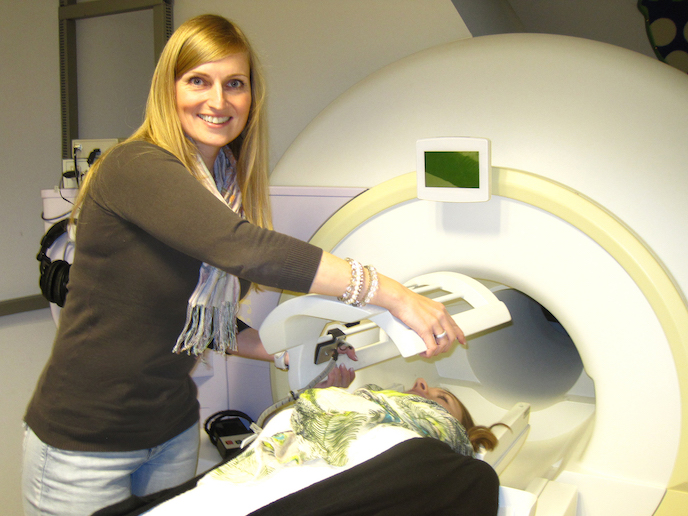
Heidi Jacobs était auparavant chercheuse au Massachusetts General Hospital de Boston(s’ouvre dans une nouvelle fenêtre) aux États-Unis, affilié à la Harvard Medical School, où une méthode spécifique a été développée utilisant l’imagerie par résonance magnétique (IRM) pour visualiser la tache bleue. «Grâce à cette méthode, nous avons pu mesurer ses propriétés structurelles liées à la quantité de neurones», explique Heidi Jacobs. «C’est ici que nous avons observé les toutes premières conséquences de l’accumulation de tau, avant même qu’apparaisse la moindre protéine Aβ ou des symptômes cliniques». En utilisant une autre technologie avancée de neuroimagerie, la tomographie par émission de positrons (TEP), avec un traceur radioactif qui s’allume lorsqu’il se lie à ces protéines dans le cerveau, l’équipe a découvert une corrélation entre un nombre plus faible de neurones dans la tache bleue et une présence plus élevée de protéine tau. «Nous disposions déjà de ces informations à travers des études post-mortem, mais n’avions jamais pu le démontrer auparavant dans les scintigraphies cérébrales humaines en direct», note Heidi Jacobs.
Une imagerie plus sophistiquée
«Au fur et à mesure que la maladie progresse,lorsque les individus présentent également une augmentation de protéines Aβ ou que nous pouvons observer des symptômes cliniques d’Alzheimer, alors ces associations deviennent plus fortes.» Les individus présentant la pire intégrité des taches bleues et une pathologie Aβ mineure montrent un déclin de la mémoire plus rapide au fil du temps, par rapport à ceux qui ont davantage de neurones et moins d’Aβ. «Les deux semblent liés», dit-elle. Les données sur les performances cognitives, y compris les tests de mémoire collectés depuis plus de 10 ans par l’étude Aging Brain à Harvard(s’ouvre dans une nouvelle fenêtre) aux États-Unis, ont été utilisées pour voir comment les individus déclinaient au fil du temps. Les 300 individus âgés de 50 à 80 ans qui composaient la cohorte étaient tous en bonne santé cognitive au début de l’étude longitudinale. L’équipe utilise actuellement le scanner IRM à champ élevé de l’Université de Maastricht qui a un champ magnétique plus élevé qu’un scanner ordinaire pour zoomer sur la tache bleue, puis observer les changements de densité des neurones de la tache bleue chez des individus de 30 ans et plus. «La beauté réside dans la combinaison des deux, car la TEP nous renseigne sur la nature moléculaire du cerveau tandis que l’IRM nous renseigne sur sa structure et sa fonction», explique Heidi Jacobs.