Induction et transmission de l'instabilité génomique après une irradiation
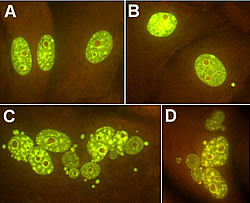
Les dommages biologiques résultant d’une exposition à des rayons ionisants sont dûs pour une bonne part au dépôt énergétique dans le noyau cellulaire ainsi qu’à l'effet ADN potentiel. Ainsi, lors de la première division cellulaire, des modifications radio-induites surviennent, alors que le clone cellulaire (entraînant des mutations dans des gènes spécifiques) est responsable des dommages. Outre ces faits connus, de récentes recherches ont révélé que des effets indirects (instabilité génomique et effets de voisinage sur cellules non irradiées) peuvent également survenir à des doses très faibles. Lors d'études épidémiologiques, la dosimétrie n'est pas toujours très précise, de sorte que des évaluations de risques faibles s'imposent. Elles ont déjà conduit à une controverse croissante sur l'adéquation des mesures de radioprotection pour les travailleurs exposés et le public. D'autre part, des modèles biologiques fournissent des données sur les effets directs des rayonnements et sur les effets non ciblés qui jouent un rôle majeur dans les régions recevant de faibles doses. C'est la raison pour laquelle les chercheurs du projet RADINSTAB ont étudié l'effet de très faibles doses par le biais de modèles cellulaires et animaux plutôt que d'études radiobiologiques classiques. ils ont étudié en détail deux mécanismes qui contribuent grandement à la réponse cellulaire. Ils ont tout d'abord démontré qu'à de faibles doses l'effet de voisinage (signalant les dommages transmis par les cellules irradiées aux cellules non irradiées) induit et préserve l'instabilité génomique. Ils ont ensuite mis en évidence qu'à de faibles doses l'hypersensibilité aux rayonnements et la radiorésistance induite, pouvant constituer un index intégré du changement de dose, affectent la relation - soit quelque 0,5-1 Gy de faible irradiation LET (transfert linéique d'énergie). Les résultats dérivés sont très intéressants. Ils montrent que l'expression de ces deux mécanismes diffère grandement alors que l'impact de doses très faibles est plus important que prévu. Les lignées de cellules à effet de voisinage important ne présentent pas de radiorésistance induite et vice versa. De plus, les lignées dont la courbe de réponse de dose d'irradiation se caractérise par un large épaulement ne présentent pas forcément HRS/IRR et effet de voisinage. Quoi qu'il en soit, les recherches sur la base génétique de cette variabilité se poursuivent. Illustration : cellules urothéliales porcines normales avec explant (A), cellules micronucléées touchées par l’effet de voisinage (B) et cellules apoptotiques (C, D) colorées à l’acridine orange (cf. Belyakov, O.V. Folkard, M., Mothersill, C., Prise, K.M. and Michael, B.D. (2003) A proliferation-dependent bystander effect in primary porcine and human urothelial explants in response to targeted irradiation. Br J Cancer, 88:5, 767-74).