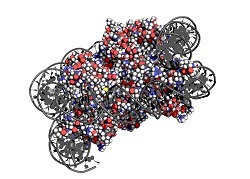
Betrachtung von Chromatin auf molekularer Ebene
Chromatin ist der Komplex aus DNA und organisierenden Proteinen, die sich im Inneren des Zellkerns befinden. Die Struktur von Chromatin ist extrem wichtig, da ein Umbau zu einer Genaktivierung oder -repression führen kann. Genkontrolle ist entscheidend für die Entwicklung von Stammzellen, in denen eine pluripotente Zelle zu einem beliebigen körpereigenen Zelltyp reifen kann. Für die Forscher ist es äußerst wichtig, diese Zellen für die Stammzelltherapie genau kontrollieren zu können. Ebenso wichtig ist die Epigenetik, bei der die Gentranskription durch die Chromatinumgebung verändert werden kann. Neuere Forschungen haben ergeben, dass die räumliche Organisation von Chromatin einen Schlüsselfaktor für die Regulierung von Gen-Silencing und der Genexpression darstellt. Die Chromatinstruktur bleibt jedoch aufgrund der verwendeten Längenskalen im Nanometerbereich und den Einschränkungen der räumlichen Auflösung, des schlechten Signal-Rausch-Verhältnisses und der Mittelwertbildung in bestehenden Verfahren schlecht aufgelöst. Gegen konventionelle Fluoreszenzmikroskopie, für SRFM Der Hauptforscher des VCSD-Projekts (Visualising chromatin structure and dynamics), Dr. Jason Otterstrom, nutzte die hochauflösende Fluoreszenzmikroskopie (SRFM), um diese Einschränkungen mithilfe der Finanzierung aus einem Marie-Curie-Stipendium zu überwinden. Aufgrund seiner langjährigen Erfahrung in der Fluoreszenzmikroskopie an biologischen Systemen arbeitete er in zwei Laboren am Institut für Photonische Wissenschaften, Barcelona, zunächst mit Melike Lakadamyali und zuletzt mit Dr. Loza-Alvarez, beide Experten für SRFM. Die verwendete Technik identifiziert die 3D-Position einzelner fluoreszierender Farbstoffe und rekonstruiert ein Bild mithilfe dieser Positionen, so ähnlich wie die Maler des Pointillismus oder der „gepunkteten Kunst“ im 19. Jahrhundert. Das übergeordnete Ziel von VCSD bestand darin, einen neuen Rahmen für die Charakterisierung der Chromatinstruktur zu schaffen. „Um dies zu erreichen, mussten wir eine Methodik und einen Algorithmus entwickeln, um hochauflösende Fluoreszenzmikroskopie-Daten in zwei Farben und in 3D zu überlagern“, erklärt Dr. Otterstrom. Durch den Algorithmus halfen die hochauflösenden Daten nach dem Chromatin-Umbau, DNA zusammen mit Histonen auf globaler Ebene zu visualisieren und zu quantifizieren. Der nächste Schritt wäre, einen definierten Genort innerhalb des Zellkerns ins Visier zu nehmen, um die Chromatinorganisation und den Chromatin-Umbau auf lokaler Ebene zu untersuchen, da diese mit der Genexpression korrelieren. Die Suche nach den perfekten Farbstoffen für mehrfarbige Bilder Die Verwendung mehrerer Farbstoffe für die Mehrfarbenabbildung brachte verschiedene Herausforderungen mit sich. „Ich fand heraus, dass manche Farbstoffe zwar für die Abbildung einiger Strukturen in der lokalisierungsbasierten SRFM einzelner Moleküle geeignet sind, jedoch für andere Strukturen, wie beispielsweise die Histone, die ich visualisieren wollte, nicht funktionieren“, betont Dr. Otterstrom. Die Antwort war, eine breite Suche nach geeigneten Farbstoffen und den erforderlichen Pufferbedingungen durchzuführen. Schließlich entstand durch die Zusammenarbeit mit einem anderen Doktoranden die Idee, eine orthogonale Einzelmolekülmethode mit einer anderen Anforderung an die Farbstoffqualität zu verwenden. „Ich musste meinen Datenfluss anpassen, um die beiden Abbildungsstrategien zusammenzuführen, aber es war erfolgreich“, berichtet Dr. Otterstrom. Zukünftige Anwendungen auf persönlicher Ebene und darüber hinaus Die Analyse der VCSD-Ergebnisse wird ebenso fortgesetzt wie die Datenerfassung. Es wird damit gerechnet, dass die entwickelte Methodik von Forschern auf den Gebieten der Stammzellen- und Chromatinbiologie übernommen und somit Europas weltweiten Ruf in der wissenschaftlichen Innovation stärken wird. „Das Marie-Curie-Stipendium ermöglichte es mir, Anwendungen im Bereich der Chromatinstrukturquantifizierung als unabhängiger biophysikalischer Forscher zu verfolgen und eine befriedigende Arbeit auf diesem Gebiet zu finden“, resümiert Dr. Otterstrom. Angesichts der zunehmenden Bedeutung des Wissens über die Chromatinstruktur auf Nanoebene bei Stammzellanwendungen und allgemein in der Epigenetik hat VCSD eine solide Wissensbasis für einen schnell wachsenden Bereich in der Biomedizin geschaffen.