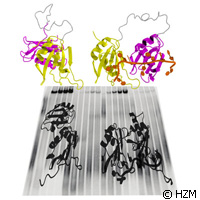
Le mécanisme humain de régulation génétique découvert
Des scientifiques allemands, espagnols et français expliquent que pour produire des protéines, il suffit de transcrire un gène d'encodage de protéine en ARN (acide ribonucléique) et qu'au cours du processus d'épissage, il convient de le raccourcir au modèle désiré. Dans leur dernière étude présentée dans la revue Nature, les chercheurs présentent de nouvelles informations sur la manière dont la protéine U2AF est impliquée dans le processus. La recherche était partiellement financée par trois projets de l'UE à hauteur de 25,4 millions d'euros au total, au titre du sixième programme-cadre (6e PC). Menés par l'Helmholtz Zentrum München et l'université technique de Munich (TUM) en Allemagne, les chercheurs ont découvert que la protéine U2AF active le pré-ARN messager (pré-ARNm), qui sert de modèle pour la synthèse protéique dans le corps. Le pré-ARNm doit tout d'abord être transcrit à partir de l'ADN (acide désoxyribonucléique). Plusieurs protéines, que les experts appellent facteurs d'épissage, doivent collaborer pour assurer le succès de l'épissage, qui joue un rôle crucial dans le système central de la biologie moléculaire. Ainsi, les informations génétiques vont dans un sens: de l'ADN à l'ARN, et de l'ARN aux protéines. Une structure spécifique est contenue dans les gènes du génome humain. Les régions avec des exons importants s'alternent aux régions que les chercheurs ont appelées introns; qui ne comportent aucune donnée importante pour l'encodage de la protéine correspondante. Certains membres de l'équipe ont évalué U2AF, qui est un facteur d'épissage composé de deux modules structurels et se lie à l'ARN à proximité de la frontière intron-exon. La copie du pré-ARNm est épissée et les introns sont éliminés. Ainsi, l'ARNm ne comprend que des exons, qui encodent la séquence d'acides aminés d'une protéine donnée. «La structure spatiale de la protéine U2AF alterne entre une conformation ouverte et fermée», explique le professeur Michael Sattler, responsable de l'Institute for Structural Biology au Helmholtz Zentrum München et professeur au Biomolecular NMR [nuclear magnetic resonance] Spectroscopy du TUM. «Une séquence d'ARN correspondante dans l'intron incite U2AF à penser qu'il s'agit d'une conformation ouverte, ce qui active l'épissage et mène au final à l'élimination de l'intron.» Selon les chercheurs, la séquence d'ARN de l'intron détermine l'activation efficace de la modification conformationnelle. Un processus de sélection conformationnelle aide à équilibrer les formes ouvertes et fermes de la protéine U2AF. L'ARN se lie à une minuscule fraction de la conformation ouverte existante, en dépit de l'absence ou de la présence d'ARN. Ils pensent que des mécanismes similaires contribueraient à la régulation d'un nombre de voies de signalisation dans la cellule. «Nos résultats indiquent que le tandem des domaines RRM de U2AF65 n'agit pas simplement en tant que support de la liaison, mais a plutôt un rôle actif dans la relation quantitative entre la force de traction de polypyrimidine, le site de reconnaissance d'épissage et l'assemblage du splicéosome», commentent les auteurs. «La sélection conformationnelle multidomaines des états ouverts permet au tandem de domaines RRM de fonctionner comme un rhéostat moléculaire par rapport à l'activité d'U2AF durant les premières étapes d'épissage, entraînant une compétition entre RRM1 et RRM2 (auto-inhibition dans une conformation fermée) et l'ARN (activation par une conformation ouverte). Il s'agit d'un filtre de sélectivité contre la liaison d'ARN défectueuse et l'assemblage du complexe d'épissage, car l'affinité élevée des ligands de voie de polypyrimidine sont plus adaptés à contrebalancer la pénalité énergétique nécessaire aux deux domaines RRM pour leur liaison.» L'étude a été financée par les projets suivants au titre du domaine thématique «Sciences de la vie, génomique et biotechnologie pour la santé» du 6e PC: 3D-REPERTOIRE, FSG-V-RNA, et EURASNET. Le projet 3D-REPERTOIRE («A multidisciplinary approach to determine the structures of protein complexes in a model organism») a reçu un financement de 13 millions d'euros. FSG-V-RNA («Functional and structural genomics of viral RNA») était soutenu à hauteur de 2,4 millions, et EURASNET («European alternative splicing network of excellence») à hauteur de 10 millions d'euros.Pour de plus amples informations, consulter: Revue Nature: http://www.nature.com/(s’ouvre dans une nouvelle fenêtre) Helmholtz Zentrum München: http://www.helmholtz-muenchen.de/en/start/index.html(s’ouvre dans une nouvelle fenêtre)
Pays
Allemagne, Espagne, France