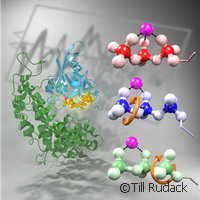
I ricercatori fanno luce sul meccanismo della proteina Ras che regola la crescita cellulare
La proteina Ras è presente in praticamente tutti gli esseri viventi ed è importante per tutte le cellule viventi. È responsabile di tante cose, ma quella più importante è forse la regolazione della crescita delle cellule. Il meccanismo molecolare attraverso il quale la proteina Ras accelera la divisione della molecola guanosina trifosfato (GTP), rallentando così la crescita della cellula, è stato adesso descritto dal Prof. Dott. Klaus Gerwert, un biofisico della Ruhr-Universität Bochum, Germania nell'edizione online della rivista PNAS. Lo sue scoperte fanno seguito all'uso combinato di spettroscopia a infrarossi e simulazioni al computer. In questo modo si è potuto mostrare che la Ras mette una catena di fosfati sotto una tale pressione che un gruppo di fosfati si può staccare molto facilmente, il freno per la crescita della cellula. La mutazione della Ras è coinvolta nella formazione dei tumori perché questa reaziona rallenta e il freno alla crescita della cellula non funziona. "Le nostre scoperte potrebbero aiutare a sviluppare piccole molecole che ripristinino la giusta velocità delle proteine Ras," dice il prof. Gerwert. "Tali molecole sarebbero interessanti anche per la terapia molecolare per il cancro." Le malattie come la leucemia mieloide cronica (LMC) attualmente si possono curare attraverso la terapia molecolare del cancro con farmaci come il Gleevec, ma non sono state ancora trovate molecole che abbiano un effetto simile sulla proteina Ras mutata. "Visto che adesso siamo in grado di studiare le reazioni della proteina Ras con una risoluzione molto migliore, si stanno formando nuove speranze che sarà possibile neutralizzare la molecola mutata usando farmaci come il Gleevec e ripristinare il ritmo della cellula," dice il prof. Gerwert. Normalmente la proteina Ras disattiva la crescita della cellula staccando un gruppo di fosfati dalla piccola molecola GTP. La GTP ha tre gruppi di fosfati collegati. Se è presente nell'acqua, il terzo gruppo di fosfati si può dividere spontaneamente, anche senza l'aiuto della proteina Ras. Il processo è però molto lento. La Ras accelera la divisione di cinque volte e una seconda proteina, chiamata GAP, di altre cinque volte. Adesso il team della Ruhr-Universität Bochum ha scoperto cosa provoca questa accelerazione. La Ras porta la catena di tre gruppi di fosfati alla GTP in una certa forma. Gira il terzo e il secondo gruppo di fosfati l'uno verso l'altro in modo che la catena sia sotto tensione. "È come dare la carica a una molla in un'automobilina giocattolo girando una vite," spiega il prof. Gerwert. "La Ras è la vite, i gruppi di fosfati formano la molla." La proteina GAP sottopone a ulteriore tensione la molla girando anche il primo gruppo di fosfati contro il secondo. In questo modo, la GTP entra in uno stato a energia così alta che il terzo gruppo di fosfati si può facilmente staccare dalla catena, in modo simile a quando un'automobile giocattolo parte spontaneamente dopo che è stata data la carica alla molla. I risultati sono stati ottenuti usando la spettroscopia a infrarossi trasformata di Fourier (FTIR) risolta nel tempo sviluppata presso l'Istituto di biofisica. Attraverso l'uso di questa tecnica, gli scienziati seguono le reazioni e le interazioni di proteine con un'alta risoluzione spaziale e temporale in modo molto più preciso che non usando un microscopio. "La spettroscopia però non fornisce fotografie belle come un microscopio, ma soltanto spettri infrarossi molto complessi," spiega il dott. Carsten Kötting del team di ricerca. "Come un codice segreto che deve essere decifrato." A causa dell'enorme sforzo computazionale, molecole grandi come una proteina completa non possono attualmente essere descritte in modo affidabile usando queste cosiddette simulazioni quantiche meccaniche. Quindi i ricercatori hanno limitato la loro analisi alla GTP e la parte della proteina Ras o GAP che interagisce direttamente con la GTP. Hanno descritto il resto delle proteine con una simulazione delle dinamiche molecolari meno elaborata. "Quando si mettono insieme tutte le diverse simulazioni, è facile essere messi fuori strada," dice Till Rudack. "Quindi bisogna controllare la qualità dei risultati confrontando gli spettri a infrarossi simulati con quelli misurati." Se gli spettri ottenuti con entrambe le tecniche corrispondono, la struttura delle proteine si può determinare con una precisione di un milionesimo di un micrometro, come mostrato nello studio della Ruhr-Universität Bochum.Per maggiori informazioni, visitare: Ruhr-Universität Bochum: http://www.ruhr-uni-bochum.de/index_en.htm(si apre in una nuova finestra) PNAS: http://www.pnas.org/(si apre in una nuova finestra)
Paesi
Germania