Proteine ospiti coinvolte nelle barriere fra specie delle infezioni virali
Si ritiene che la maggior parte dei coronavirus (CoV) umani sia emersa tramite trasmissione zoonotica e si sia adattata all’ospite umano. Sebbene la maggior parte sia causa di infezioni del tratto respiratorio superiore lievi, la grave sindrome respiratoria acuta da coronavirus (SARS-CoV, Severe Acute Respiratory Syndrome Coronavirus), la sindrome respiratoria del Medio Oriente da coronavirus (MERS-CoV, Middle East Respiratory Syndrome) e il più recente coronavirus(si apre in una nuova finestra) (nCoV2019) di Wuhan, in Cina, hanno dimostrato che il potenziale dei CoV è altamente patogeno.
Uno schermo genetico per identificare i fattori di restrizione dei CoV
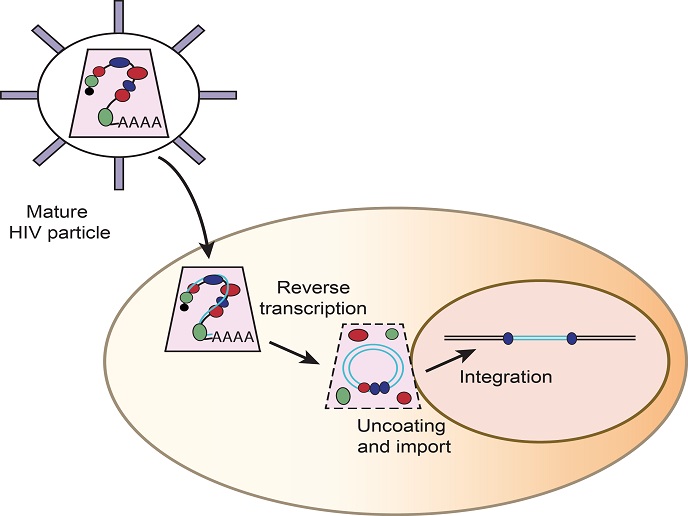
Con il supporto del programma Marie Skłodowska-Curie, il progetto COV RESTRIC ha studiato i meccanismi che consentono ai CoV di superare le barriere fra specie. «Il nostro obiettivo era quello di determinare quali meccanismi ospiti impediscono la trasmissione attraverso diverse specie e identificare gli eventuali fattori particolari implicati nel processo», spiega il coordinatore del progetto Volker Thiel, professore di virologia presso l’Università di Berna. Il suo team ha lavorato con l’ipotesi che i fattori di restrizione limitino la replicazione virale in diverse specie. Le infezioni zoonotiche diventano possibili quando i virus sfuggono ai meccanismi di restrizione antivirale e adattano le loro strategie al nuovo ospite. Per identificare le proteine ospiti che limitano la replicazione del CoV, i ricercatori hanno combinato tecnologie all’avanguardia con uno schermo genetico su diverse centinaia di geni stimolati dall’interferone (ISG, Interferon-Stimulated Genes). Gli ISG codificano effettori antivirali che potrebbero agire come fattori di restrizione virale e sono stimolati dalla risposta dell’interferone di tipo I nota per il suo ruolo protettivo contro i patogeni. Lo schermo genetico ha rivelato una serie di geni in grado di limitare la replicazione di diverse varianti di CoV in varie cellule ospiti. Una particolare proteina ospite, l’antigene linfocitario 6 del locus complesso E (LY6E), ha dimostrato un’elevata efficacia nel bloccare l’ingresso di CoV nelle cellule ospiti. I ricercatori hanno studiato la conservazione di LY6E testando geni ortologhi provenienti da macaco rhesus, topo, pipistrello e cammello. È interessante notare che tutte le varianti ortologhe di questo gene hanno inibito l’infezione da CoV umano, indicando che questa funzione di LY6E è conservata tra le specie. Inoltre, gli scienziati hanno convalidato l’attività antivirale di LY6E in vari modelli umani e murini di infezione da CoV, dove hanno osservato la capacità di questa proteina ospite di proteggere le cellule immunitarie da diversi virus, tra cui MERS-CoV e SARS-CoV. Animali privi di LY6E presentavano una vulnerabilità all’infezione da CoV, con macrofagi e cellule B gravemente colpiti.
Significato clinico dei risultati di COV RESTRIC
I risultati di COV RESTRIC indicano la presenza di alcune proteine ospiti che proteggono specificamente le cellule immunitarie dall’infezione da virus. «Soprattutto, il nostro lavoro sottolinea l’importanza della protezione delle cellule immunitarie dalle infezioni virali», sottolinea Stephanie Pfänder, borsista Marie Skłodowska-Curie. I piani futuri includono chiarimenti sul meccanismo mediante il quale LY6E offre un’ampia protezione antivirale. Dati preliminari indicano che la proteina funziona bloccando l’ingresso del virus, ma sono necessari ulteriori esperimenti per studiare l’attività di LY6E nel contesto dell’interazione delle cellule immunitarie durante una risposta immunitaria. I partner hanno anche in programma di studiare altri geni candidati ISG che limitano la replicazione del CoV. La nuova attività inibitoria dell’ISG LY6E contro i CoV altamente patogeni ha il potenziale per condurre a nuove strategie di protezione delle cellule immunitarie dalle infezioni. Considerando la grave malattia e l’elevata mortalità associate all’infezione da SARS-CoV e MERS-CoV e la recente comparsa di un nuovo CoV nel 2019 a Wuhan, in Cina, l’impatto clinico di COV RESTRIC è importante. In prospettiva, Thiel prevede di «sfruttare ulteriormente la conoscenza dei meccanismi intrinseci di difesa dell’ospite conservati su più specie per lo sviluppo di nuove opzioni terapeutiche contro altri virus».