Probacteriófagos: un nuevo agente para la transferencia de genes de resistencia a los antibióticos
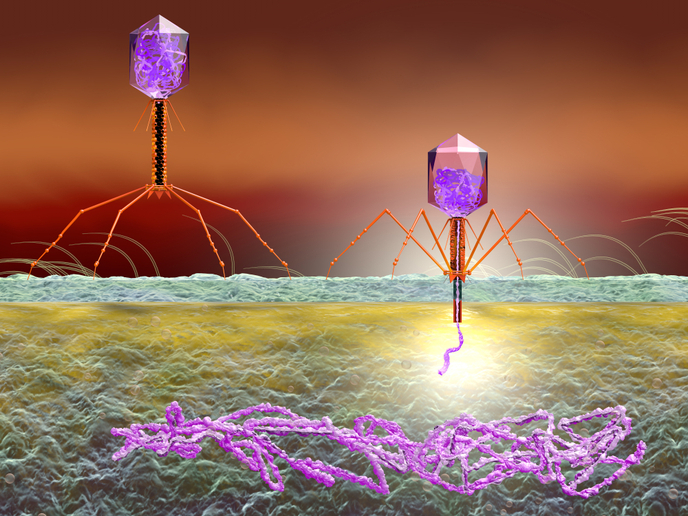
Los bacteriófagos(se abrirá en una nueva ventana) son virus que infectan bacterias y tienen un ciclo de vida lítico o lisogénico(se abrirá en una nueva ventana). En el ciclo lítico, los bacteriófagos se multiplican y liberan nuevos viriones que usan las células hospedadoras, mientras que en el ciclo lisogénico, los bacteriófagos incorporan su propio material genético al cromosoma bacteriano, formando probacteriófagos(se abrirá en una nueva ventana). Este mecanismo facilita la transferencia de genes nuevos a las bacterias, incluidos genes de resistencia a los antibióticos (ARG, por sus siglas en inglés), lo que contribuye a que las bacterias se adapten a las nuevas condiciones ambientales. Sin embargo, no se sabe a ciencia cierta cómo evolucionan los probacteriófagos portadores de (ARG).
Evaluar los costes y los beneficios de la eficacia biológica de los probacteriófagos para las células hospedadoras
El proyecto ProphARG se propuso investigar cómo los probacteriófagos influyen en la eficacia biológica bacteriana. Realizado con el apoyo de las Acciones Marie Skłodowska-Curie(se abrirá en una nueva ventana) (MSCA), en el proyecto se diseñaron experimentos con los que estudiar la evolución de los probacteriófagos portadores de genes de resistencia a los antibióticos y su impacto en la bacteria hospedadora «Escherichia coli». «Nuestro objetivo fue estudiar el efecto de los probacteriófagos en hospedadores bacterianos en términos de resistencia a los antibióticos y enfermedades infecciosas en humanos y animales», explica Carolin Charlotte Wendling, beneficiaria de una subvención de las MSCA. El equipo, con la intención de cuantificar la eficacia biológica relativa de las bacterias, realizó ensayos de competencia por pares entre bacterias que contienen un probacteriófago y otras sin probacteriófago. Para poder derivar conclusiones generales de una amplia gama de genes de resistencia y tipos de bacteriófagos, utilizaron probacteriófagos artificiales en lugar de naturales, donde una región genómica no esencial del bacteriófago se sustituyó por un ARG. Se llevaron a cabo ensayos de competencia en múltiples entornos para diferenciar entre los efectos de la eficacia biológica de los probacteriófagos portadores de ARG y lo que no los tienen. Los resultados obtenidos mostraron que las condiciones ambientales regían los beneficios o el coste de eficacia biológica de los probacteriófagos a las bacterias hospedadoras. En ausencia de antibióticos u otras condiciones estresantes, los ARG y los probacteriófagos no suponían costes para sus anfitriones. En condiciones que favorecen el ciclo lítico, como la exposición a la luz ultravioleta u otros agentes que dañan el ADN, la eficacia biológica de las bacterias con probacteriófagos fue mayor que la de aquellas sin probacteriófagos. Esto se debió a que los probacteriófagos volvieron al ciclo lítico y mataron a las bacterias libres de bacteriófagos competidores. Por el contrario, en presencia de antibióticos, las bacterias con probacteriófagos portadores de ARG sobrevivieron mejor ya que pudieron resistir a los antibióticos. «Los ARG se volvieron ventajosos a concentraciones más altas de antibióticos», enfatiza Wendling.
Impacto clínico de ProphARG
Las bacterias resistentes a múltiples fármacos representan una amenaza clínica significativa, pues restan eficacia a los antibióticos existentes y ponen en riesgo a miles de personas que realizan procedimientos rutinarios. Se sabe desde hace mucho tiempo que los bacteriófagos tienen efectos protectores sobre el hospedador, confieren inmunidad contra los bacteriófagos superinfectantes y les ayudan a resistir los antibióticos a través de ARG beneficiosos. Además, los probacteriófagos, que constituyen hasta el 20 % de los genomas bacterianos, contribuyen a la diversidad genómica entre los aislados bacterianos. Los hallazgos de ProphARG subrayan la contribución de los probacteriófagos como agentes causantes de la transferencia de ARG, donde hasta ahora, la investigación se había centrado principalmente en los plásmidos. Las concentraciones subinhibidoras de antibióticos parecen favorecer la transferencia horizontal de ARG codificados por bacteriófagos y contribuir a la propagación de la resistencia a los antibióticos. Por lo tanto, las estrategias de tratamiento con antibióticos deben adaptarse para reducir el riesgo de inducir probacteriófagos y la transferencia de ARG a otros miembros de la población bacteriana. Comprender los factores determinantes de la eficacia biológica bacteriana puede ayudar a predecir la propagación de ARG desde entornos agrícolas o naturales a la microbiota humana o patógenos. De cara al futuro, Wendling tiene como objetivo «ampliar los hallazgos de ProphARG mediante el estudio de la influencia de los probacteriófagos en la propagación de plásmidos resistentes a múltiples fármacos en comunidades bacterianas».