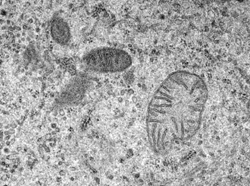
Entwicklung der Energieproduktion in der Zelle
Blastocystis ist ein einzelliger Parasit, der im Darm lebt. Da er ein strikt sauerstoffunabhängiger Organismus ist, nahmen Wissenschaftler an, dass die Energieproduktion der Zelle in einem sogenannten Hydrogenosom abläuft. In jüngster Zeit wurde jedoch erkannt, dass Blastocystis über einen intermediären Organellentypus verfügt, eine Mitochondrium-ähnliche Organelle (MRO). Vorhergehende Untersuchungen deuten darauf hin, dass die MRO sowohl über metabolische Merkmale verfügt, die bei Hydrogenosomen vorkommen als auch über solche, die Gemeinsamkeiten mit Mitochondrien aufweisen. Aus evolutionärer Sicht ist dies eine einzigartige Möglichkeit, die Entwicklung der Mitochondrien zu untersuchen. Mit molekularen Hilfsmitteln sowie Instrumenten aus den Bereichen der Zellbiologie und der Bioinformatik wollte man im Projekt "Evolution and function of the Blastocystis mitochondrion-like organelle" (BHMLOEVOFUNC) die Funktionen der Blastocystis-MRO untersuchen und die Organelle beschreiben. Sequenzmarker, sogenannte Expressed Sequence Tags (EST), sind eine kurze komplementäre DNA-Sequenz. Mithilfe dieser EST konnten Wissenschaftler die Funktionen der MRO und mögliche Anpassungen an einen anaeroben Lebensstil vorausberechnen. Die Forscher bestimmten je 115 bzw. 360 Gene, die mögliche mitochondriale bzw. hydrogenosomale Proteine programmieren sowie mindestens 412 MRO-Proteine. Ein neues vom Team entwickeltes Protokoll analysierte die Organelle, um ihre Funktionen zu bestimmen. Für die Datenanalyse wurde Mascot- und Paragon-Software eingesetzt, und man konnte rund 150 Proteine bestimmen. Vorläufige Ergebnisse deuten darauf hin, dass die Biosynthesewege mit den Prognosen der EST-Analyse übereinstimmen, und man plant, diese Daten im Laufe der weiteren Arbeiten zu bestätigen. Eisen-Schwefel-Proteincluster (Fe-S) sind aufgrund ihrer Bedeutung für den mitochondrialen Elektronentransport weitbekannt. Nach der Theorie, dass sich frühe Lebensformen auf der Oberfläche von Eisen-Schwefel-Mineralien gebildet haben, werden sie mit dem Ursprung des Lebens in Verbindung gebracht. BHMLOEVOFUNC untersuchte den Mechanismus der Fe-S-Cluster, und man fand in den meisten anderen MRO viele Homologien der Kernproteine. Das Kernprotein Isa2 kann beispielsweise ein funktional vergleichbares Protein im Parasiten ersetzen, das die Schlafkrankheit verursacht. Darüber hinaus entdeckte man ein neues Fe-S-Cluster zur Mobilisierung von Schwefel, das aus einem lateralen Gentransfer aus methanbildenden Archaebakterien gewonnen wurde. Von dieser Gattung leben viele in extremen Bedingungen, wie beispielweise in heißen Quellen, indem sie unter sauerstofffreien Bedingungen Methan produzieren. Die Projektergebnisse könnten über die bislang unbekannten Funktionen der energieproduzierenden Organelle dieses anaeroben Parasiten Aufschluss geben. Auf diese Weise gewinnen wir Erkenntnisse über die Evolution und die Vielfalt des anaeroben Stoffwechsels sowie über die Vielfältigkeit eines Stützpfeilers des Lebens, des Mitochondriums.