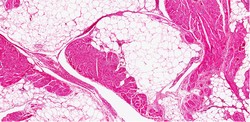
Die molekulare Ätiologie der kardialen Hypertrophie
Eine kardiale Hypertrophie beinhaltet eine Vergrößerung und Verdickung der Herzwand. Dies kann sich zunächst als vorteilhaft erweisen, da eine erhöhte Leistung möglich ist. Letztlich kann diese Entwicklung jedoch schädlich sein und in Kardiomyopathie, Herzversagen und Sekundentod resultieren. Das hypertrophe Wachstum ist von der Fähigkeit adulter Kardiomyozyten abhängig, auf eine Vielzahl mitogener Reize zu reagieren, welche die Zellzyklusprogression vorantreiben. Im Zuge neuer Forschungsarbeit wurde die Helikase CHAMP als wichtiger Regulator für die Kardiomyozytenproliferation mit antihypertrophen Eigenschaften ermittelt. Es zeigte sich, dass CHAMP ein konserviertes ATPase-Motiv-Charakteristikum von RNA-Helikase-Superfamilien beinhaltet und mit Zellzyklusinhibitoren interagiert. Im Hinblick auf den molekularen Mechanismus, über den RNA-Helikasen die Translation regulieren, ist allerdings nur sehr wenig bekannt. Das oberste Ziel des EU-finanzierten Projekts CHAMP RNA HELICASE (Function, mechanism, and regulation of mammalian Mov10L1 RNA helicase) bestand darin, den molekularen CHAMP-Mechanismus und das Verhältnis zwischen Struktur und Funktion zu entschlüsseln. Die Forscher waren insbesondere an den spezifischen und unspezifischen RNA-Substraten interessiert, die das CHAMP-Polypeptid zur Vermittlung seiner RNA-Remodellierungsfunktion aktiviert. Im Zuge der Forschungsaktivitäten wurden hochmoderne Ansätze aus den Bereichen Biochemie und Biophysik angewandt und auf die Regulation von Genen fokussiert, die für die Entwicklung des Herzens während der pränatalen und postnatalen Entwicklungsstufen von entscheidender Bedeutung sind. Darüber hinaus beleuchteten Wissenschaftler die Bedeutung von CHAMP für den RNA-Metabolismus in der Zelle. Die Resultate legen nahe, dass die Helikase sehr wahrscheinlich die Ziel-RNA auf der Translations- und Degradationsebene reguliert. Im Hinblick auf die Translation lässt dies darauf schließen, dass CHAMP die mRNA von Zellzyklusinhibitoren in der postnatalen Phase der Herzentwicklung reguliert. Abgesehen von fundamentalen Erkenntnissen über den regulatorischen Mechanismus bei einer Kardiomyozytenhypertrophie legen die Ergebnisse nahe, dass CHAMP bei einer kardialen Hypertrophie als Therapieziel mit signifikanten klinischen Implikationen fungieren könnte.