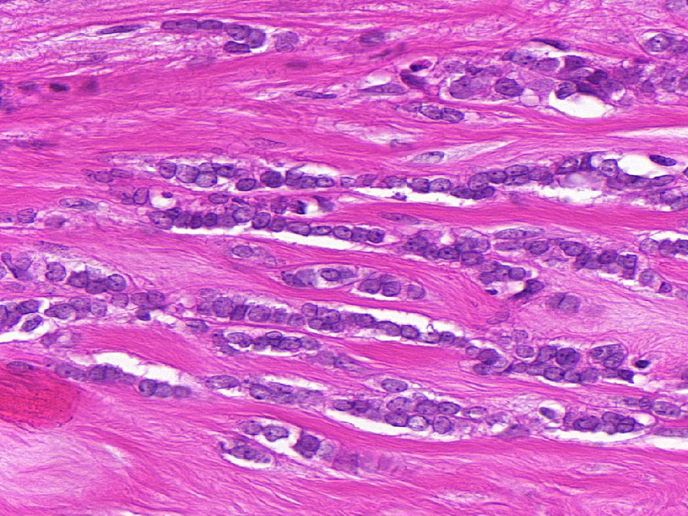
Diagnósticos y tratamientos precisos para cánceres difíciles de tratar
El genotipado relacionado con el cáncer ha correlacionado las respuestas a fármacos oncológicos específicos con mutaciones de determinados genes. Muchas de estas mutaciones se producen en unos componentes de señalización, denominados quinasas. Los subtipos de carcinoma lobular invasivo (CLI) o el cáncer de mama triple negativo (TN), ambos difíciles de tratar y que representan el 25 % de todos los cánceres de mama, carecen actualmente de terapias específicas, lo cual da lugar a un mal pronóstico para las pacientes. El proyecto financiado con fondos europeos RATHER (Rational Therapy for Breast Cancer: Individualized Treatment for Difficult-to-Treat Breast Cancer Subtypes) desarrolló firmas de biomarcadores específicas para predecir la evolución en pacientes con CLI (empleando la prueba MammaPrint) o la respuesta a la terapia en pacientes con cáncer de mama TN (empleando la prueba BRCAness), y descubrió tratamientos novedosos para ambos subtipos de cáncer de mama. Los resultados de RATHER tienen un potencial clínico inmediato para ampliar el alcance de MammaPrint (una prueba diagnóstica ya aprobada) al subgrupo de cánceres de mama con CLI. El proyecto ha contribuido, asimismo, a varios ensayos clínicos, cuyo trabajo ha dado lugar a nuevos métodos terapéuticos y de diagnóstico que ahora allanan el camino a nuevos avances en el tratamiento del cáncer de mama. Adaptación de la medicina Muchos tipos de cáncer modifican unas proteínas celulares clave denominadas quinasas. Además de desempeñar una función fundamental en las vías fisiológicas, en lo que respecta al cáncer, la quinasas actúan como interruptores moleculares para controlar su crecimiento y propagación. RATHER investigó los genes que producen las proteínas quinasas para determinar si unos cambios específicos en el código de los genes u otras alteraciones en las células cancerígenas de la paciente, pueden explicar por qué se forma y extiende el cáncer. RATHER investigó la tasa de activación de todas las quinasas (el «quinoma») en tumores de mama TN que carecen de los receptores para estrógenos, progesterona y HER2 (el 15 % de los cánceres de mama) y en CLI de mama (el 10 % de los tumores de mama). Más concretamente, se secuenciaron 518 genes de quinasas para identificar mutaciones relacionadas con cualquiera de estos cánceres de mama. Además de la secuenciación del ADN, se evaluaron las alteraciones de las quinasas a escala del ARNm y las proteínas, así como los indicios de variaciones en el número de copias. Para analizar las alteraciones, se utilizaron sistemas informáticos y modelos de laboratorio preclínicos. Tal y como explica el coordinador de proyecto, el profesor William Gallagher: «Nuestro trabajo ha identificado diferencias en cánceres de mama de distintos subtipos y se basa en el hecho de que algunas de estas alteraciones resultarán estar implicadas en la propagación de la enfermedad y no ser únicamente efectos aleatorios». Cuando estaban presentes, se seleccionaron pequeñas moléculas inhibidoras según su capacidad de limitar el crecimiento de las células que expresan alteraciones de quinasas específica de estos subtipos. El consorcio de RATHER desempeñó un papel principal en un ensayo clínico de fase Ib/II llevado a cabo en varios centros sobre un novedoso medicamento inhibidor de quinasas denominado «taselisib». La fase inicial Ib del ensayo logró mostrar que las pacientes toleraban adecuadamente una combinación de la terapia endocrina tradicional (el medicamento tamoxifeno) y este nuevo inhibidor de quinasas. Tal y como resume el profesor Gallagher: «Al desvelar los cambios que tienen lugar en determinadas quinasas y la función de la proteína mutada, y localizarlos posteriormente en el subtipo de cáncer de mama específico de la paciente, descubrimos varias formas nuevas de predecir con precisión la evolución y también de tratar a las pacientes de ese subtipo con más eficacia». RATHER contribuye directamente a desarrollar aplicaciones que no solo facilitarán un mejor diagnóstico, sino también opciones terapéuticas para el cáncer de mama, una de las principales de causas de muerte relacionada con el cáncer en las mujeres. El trabajo de RATHER se alinea con esfuerzos más amplios hacia un tratamiento más individualizado del cáncer. La fase II del ensayo clínico del nuevo inhibidor de quinasas está actualmente en curso junto con ensayos complementarios.