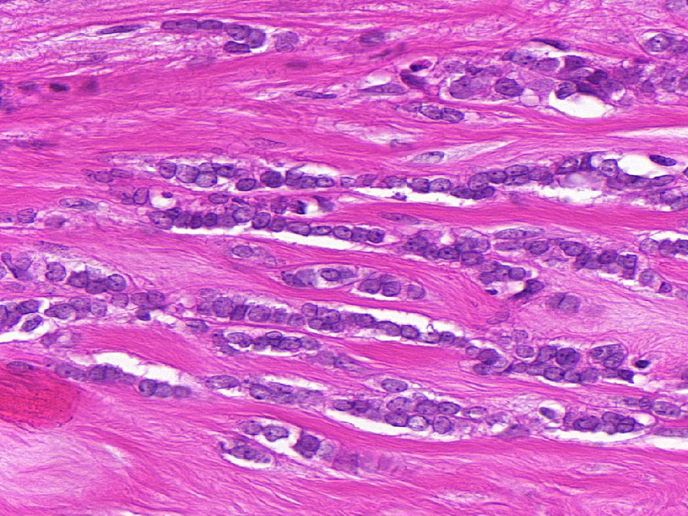
Diagnostic de précision et traitement pour les cancers difficiles à traiter
Le génotypage du cancer a corrélé les réponses aux médicaments anticancéreux ciblés avec des mutations de gènes spécifiques. Nombre de ces mutations se produisent dans des composants de signalisation appelés kinases. Les sous-types difficiles à traiter du carcinome lobulaire invasif (CLI) ou du cancer du sein triple négatif (TN), qui représentent 25 % de tous les cancers du sein, manquent actuellement de traitements ciblés, conduisant à un mauvais pronostic de la patiente. Le projet RATHER (Rational Therapy for Breast Cancer: Individualized Treatment for Difficult-to-Treat Breast Cancer Subtypes), financé par l’UE, a élaboré des signatures de biomarqueurs spécifiques permettant de prédire avec précision le résultat chez les patientes présentant un CLI (avec le test MammaPrint) ou la réponse au traitement d’une patiente atteinte d’un cancer du sein TN (avec le test BRCAness), ainsi que de nouveaux traitements non couverts pour les sous-types de cancer du sein. Le potentiel clinique des résultats de RATHER est immédiat pour étendre la portée de MammaPrint (un test de diagnostic déjà approuvé) dans le sous-groupe des cancers du sein CLI. Le projet a également contribué à plusieurs essais cliniques, les travaux produisant de nouvelles approches diagnostiques et thérapeutiques, et ouvrant la voie à des avancées dans le traitement du cancer du sein. Adapter le médicament De nombreux cancers modifient les protéines cellulaires clés appelées kinases. En plus de jouer un rôle clé dans les voies physiologiques, les kinases agissent comme des commutateurs moléculaires contrôlant la croissance et la propagation du cancer. RATHER a étudié les gènes à l’origine des protéines kinases pour déterminer si des modifications spécifiques du code génétique, ou d’autres modifications des cellules cancéreuses d’une patiente, peuvent expliquer la formation et la propagation du cancer. RATHER a examiné le taux d’activation des kinases (le «kinome») dans les tumeurs du sein TN dépourvues de récepteurs œstrogènes, de progestérone et HER2 (15 % des cancers du sein) et de CLI du sein (10 % des tumeurs du sein). Plus particulièrement, 518 gènes de kinases ont été séquencés pour identifier des mutations associées à l’un ou l’autre de ces cancers du sein. En plus du séquençage de l’ADN, les altérations des kinases ont également été évaluées au niveau des ARNm et des protéines afin notamment de démontrer la variation du nombre de copies. Les modifications ont été examinées par des systèmes informatiques et via des modèles laboratoires précliniques. Le professeur William Gallagher, coordinateur du projet, explique: «Notre travail a identifié des différences dans les cancers du sein de différents sous-types et est basé sur le fait que certaines de ces altérations auront des implications dans le développement de la maladie, au delà de simples effets aléatoires». Lorsque cela était possible, les inhibiteurs de petites molécules ont été sélectionnés en fonction de leur capacité à limiter la croissance des cellules exprimant des altérations de kinases spécifiques à un sous-type. Le consortium RATHER a joué un rôle de premier plan dans un essai clinique multicentrique de phase Ib/II portant sur un nouveau médicament inhibiteur de la kinase appelé «taselisib». L’essai initial de phase Ib a montré avec succès qu’une combinaison d’un traitement endocrinien traditionnel (le médicament tamoxifène) et de ce nouvel inhibiteur de kinase était bien tolérée par les patientes. Comme le résume le professeur Gallagher, «en découvrant les modifications apportées à des kinases particulières et à la fonction de la protéine mutée, puis en remontant au sous-type spécifique du cancer du sein de la patiente, nous avons découvert plusieurs nouvelles façons de prédire avec précision les résultats pour les patientes et potentiellement de traiter plus efficacement les patientes présentant ce sous-type». RATHER contribue directement aux applications qui fourniront non seulement des diagnostics améliorés, mais également des options thérapeutiques pour le cancer du sein, l’une des principales causes de décès liés au cancer chez les femmes. Le travail de RATHER s’aligne sur les efforts plus larges visant à un traitement plus individualisé du cancer. L’essai clinique de phase II du nouvel inhibiteur de kinase est actuellement en cours parallèlement à des essais complémentaires.