La forme des protéines affectant les mutations détermine leur activation dans certaines leucémies infantiles
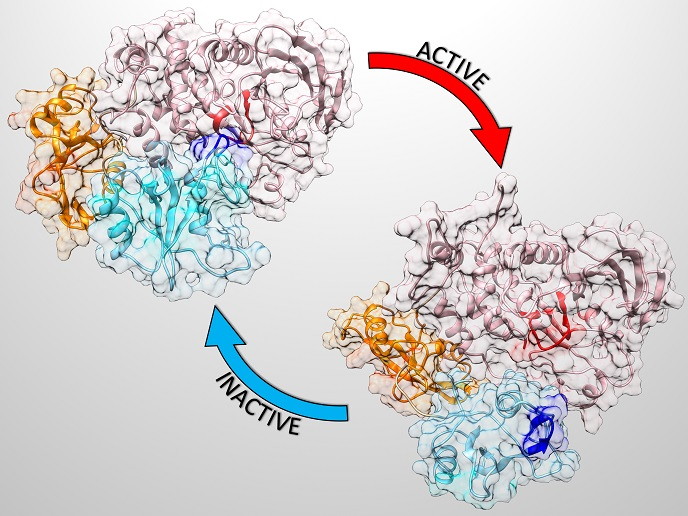
Les protéines sont des molécules complexes qui jouent des rôles essentiels dans l’organisme. La protéine SHP2 régule positivement les processus cellulaires, à tel point que ses mutations provoquent de graves troubles du développement comme le syndrome de Noonan(s’ouvre dans une nouvelle fenêtre). Les mutations du gène SHP2 engendrent également la leucémie myélomonocytaire juvénile et sont constatées plus rarement dans d’autres tumeurs malignes hématologiques. La SHP2 existe principalement sous une forme autoinhibée (inactive), et n’est complètement activée qu’après association spécifique avec ses partenaires de liaison. Veuillez consulter l’image ci-dessus pour observer les formes, très différentes, des protéines actives et inactives.
La fonction protéique et les médicaments pour contrôler les mutations
«Le projet MARS a révélé, à l’échelle atomique, les circonstances gouvernant l’activation de la SHP2. En outre, nous avons élaboré un modèle atomistique qui explique la manière dont certaines mutations liées à des maladies perturbent ce mécanisme», souligne le professeur Jochen Hub, coordinateur du projet. Atteindre ces objectifs est une importante condition préalable pour la conception de médicaments interférant de manière spécifique avec les mutants SHP2 et modulant leur fonction. Le domaine N-SH2 est la zone ou le domaine protéique qui reconnaît les partenaires de liaison essentiels et bloque le site actif de la SHP2 dans la structure autoinhibée. «Nous avons constaté que le N-SH2 adopte deux formes ou conformations distinctes; seule l’une d’entre elles a un effet activateur», explique le Dr Massimiliano Anselmi, membre du projet titulaire d’une bourse Marie Skłodowska-Curie. Curieusement, les chercheurs ont également découvert que l’activation n’est pas simplement favorisée par la simple liaison d’un chimie(s’ouvre dans une nouvelle fenêtre) (ligand), comme on le pensait auparavant, mais plutôt par le changement de la population du N-SH2, passant de la conformation ou de la forme non activatrice à l’activatrice. Cela signifie que la séquence du ligand et même sa façon particulière de se placer dans le site de liaison sont des aspects fondamentaux dans la sélection de la conformation activatrice du N-SH2.
Problèmes digestifs et défis
Les simulations soutenant de plus en plus le modèle d’activation du N-SH2, l’équipe s’est rendu compte que la plupart des données expérimentales disponibles auparavant ne pouvaient pas être interprétées clairement. «Même si rien n’avait réellement contredit nos conclusions, rien ne semblait les confirmer définitivement», se souvient le Dr Anselmi. Le problème essentiel, explique-t-il, «est que les séquences peptidiques activant le N-SH2 sont également digérées en partie (plus précisément: déphosphorylés) par le N-SH2, ce qui rend très difficile une interprétation quantitative des expériences». La réponse est venue d’une mutation signalée il y a plus de dix ans. «Nous avons constaté que les effets structurels de cette mutation pathogène concernent la région du N-SH2 qui se réorganise lors de l’activation et pouvaient s’expliquer clairement uniquement à l’aide de notre modèle», s’enthousiasme-t-il. «C’était un travail décisif et incroyable», ajoute le professeur Hub.
Clarifier les étapes floues et à venir pour comprendre le mécanisme d’activation
Les connaissances du mécanisme d’activation de la SHP2 et la possibilité de l’induire artificiellement dans le cadre d’expériences en laboratoire permettent de répondre à des questions supplémentaires. Le Dr Anselmi en cite seulement un exemple: «À l’aide de données issues de la diffusion des rayons X aux petits angles (SAXS), il sera possible d’identifier la structure tridimensionnelle de l’état ouvert de la SHP2, validant ainsi la voie d’activation proposée». Les conclusions formulées par le projet MARS ont remis en question et rejeté plusieurs points de vue courants sur l’activation de la SHP2. «Souvent, d’énormes quantités de données indiquées dans la littérature se trouvent dispersées et sont quelque peu confuses; un modèle contribue à les organiser et à les établir de manière rationnelle», résume le professeur Hub.