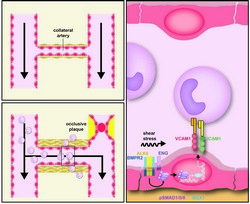
Einblicke in die endotheliale Vielfalt
EZ finden sich an der Innenwand von Blut- und Lymphgefäßen und bilden eine Schnittstelle zwischen der Gefäßwand und dem zirkulierenden Blut oder der Lymphe. Sie zeigen eine signifikante Heterogenität auf der molekularen, morphologischen und funktionellen Ebene, und zwar aufgrund sowohl von Zell-intrinsischen und -extrinsischen Faktoren. Diese Heterogenität kann die zugrunde liegende Ursache von Gefäßbett-beschränkten Störungen sein und könnte die Nebenwirkungen und den nur begrenzten Erfolg von allgemeinen (anti-)angiogenen Therapien erklären. Das EU-geförderte Projekt IMAGINED (Integrated multi-disciplinary approach to gain insight into endothelial diversity) wollte neue Erkenntnisse zur EZ-Vielfalt schaffen, um die Entwicklung von spezifischeren vaskulären Therapien zu fördern. Hierfür wählten die Forscher einen multidisziplinären Ansatz auf der Basis von Stamm-/Vorläuferzellen und Kleintiermodellen. Die Wissenschaftler analysierten das genetische Profil von arteriellen, venösen und lymphatischen EZ (makrovaskulär) sowie EZ von Herz-, Gehirn- und Leberkapillaren (mikrovaskulär). Für jede dieser EZ-Subtypen identifizierten sie innerhalb dieser Profile eine Reihe von spezifischen Transkriptionsfaktoren. Wenn sie für arterielle oder Herz-EZ spezifische Transkriptionsfaktoren in endothelialen (Progenitor-)Zellen überexprimierten, sie Zellen, erhielten sie erfolgreich Zellen mit den funktionellen und molekularen Eigenschaften des entsprechenden EZ-Subtyps. Darüber hinaus validierte das Konsortium die Rolle von zwei arteriellen und zwei Herz-endothelialen Transkriptionsfaktoren in murinen und humanen Geweben. Nach der Manipulation ihrer Expression in Zebrafischen und Mäusen demonstrierten sie auch die funktionelle Bedeutung dieser Transkriptionsfaktoren in den entsprechenden vaskulären Betten. Zusammen genommen lieferten die Untersuchungen von IMAGINED grundlegende Einblicke in die molekularen und funktionellen Eigenschaften von mikrovaskulären und makrovaskulären EZ. Die identifizierten Unterschiede könnten zur Entwicklung neuer Therapien als Grundlage dienen, sowie für die künftige Nutzung der Regenerationsfähigkeit von prä-spezialisierten EZ-Progenitoren als Therapie zum Beispiel gegen kardiale Ischämie.