Neues von AutoPilot-Dx: Neue biomarkerbasierte Assay-Technologie im Kampf gegen COVID-19 nutzen
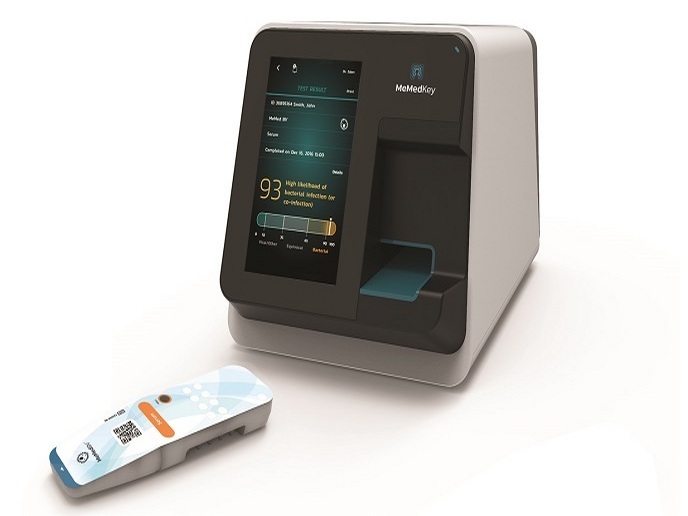
Nach der erfolgreichen Entwicklung des neues Assays beschäftigten sich die Partner von AutoPilot-Dx (Fast tracking market adoption of a novel immune-based diagnostic for improving antibiotic stewardship: automation, piloting and health economics) mit der Entwicklung einer patientennahen Plattform namens Key, dank der der Test jederzeit und überall durchgeführt werden kann und innerhalb von 15 Minuten ein Ergebnis liefert. Ausschlaggebend hierfür ist eine BV-Signatur, die auf drei als Wirt dienenden Proteinbiomarkern beruht, welche unterschiedlich auf bakterielle und virale Infektionen reagieren. „Das ist unterdessen abgeschlossen. Außerdem wurde eine CE-Kennzeichnung erteilt und wir rechnen noch 2021 mit der FDA-Zulassung“, sagt Gottlieb. „Heute wird die Key-Plattform, die den BV-Test durchführt, bereits routinemäßig in ersten medizinischen Zentren in Deutschland und Israel eingesetzt.“
Ein weiterer Mitstreiter im Kampf gegen COVID-19
Damit BV und Key weiterentwickelt werden konnten, erhielt MeMed Diagnostics eine zweite EU-finanzierte Förderung und startete das Projekt DECODE. „Mit dem Projekt sollte eigentlich unsere im Rahmen von AutoPilot-Dx getätigte Arbeit fortgeführt werden. Als die Pandemie jedoch fortschritt, wollten wir lieber untersuchen, wie BV-Biomarker für das Patientenmanagement bei COVID-19 eingesetzt werden könnten“, erklärt Gottlieb. „Die Kommission wollte diese Bemühungen unterstützen und hat der Neuausrichtung des Projekts daher gern zugestimmt.“ Im Rahmen von DECODE hat das MeMed-Team 2020 bei der Entwicklung eines neuen Produkts mitgewirkt, mit dem sich die Schwere einer COVID-19-Erkrankung frühzeitig erkennen lässt. Die Grundlage hierfür bildeten Daten, die von medizinischen Zentren in Deutschland, Israel und den Vereinigten Staaten erhoben wurden. „Mithilfe von maschinellem Lernen haben wir eine neue Signatur abgeleitet, welche die drei ursprünglichen BV-Biomarker umfasst und die Wahrscheinlichkeit angibt, nach der an SARS-CoV-2 Erkrankte einen schweren Verlauf samt Sepsis, Lungenversagen und Sterblichkeit entwickeln“, so Gottlieb weiter. „Die neue Signatur bildet die Basis für ein Produkt namens „MeMed COVID-19 Severity“. Aktuell tragen wir Proben von SARS-CoV-2-Patientinnen und -Patienten zusammen, um sie klinisch zu validieren.“ MeMed rechnet damit, dass sie im zweiten Quartal des Jahres 2021 die Zulassung in Europa und den Vereinigten Staaten beantragen können. Darüber hinaus arbeitet das Unternehmen auch daran, dass seine Tests mit dem gesamten Blut kompatibel sind, da dafür aktuell Serum notwendig ist. Dadurch könnten auch weitere klinische Einrichtungen von MeMed BV und MeMed COVID-19 Severity profitieren. „Die EU-Finanzierung hat entscheidend zur Entwicklung unserer Produkte beigetragen. Dadurch können wir über kurz oder lang Betroffenen helfen und das Gesundheitswesen der EU im Allgemeinen verbessern“, so Gottlieb abschließend.