Stopp im Namen der Neutrophilen!
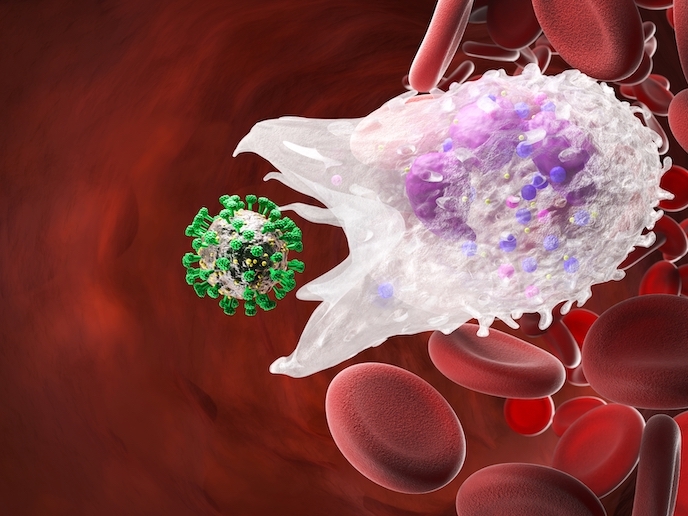
Neutrophile, die eine wichtige Rolle bei der Immunabwehr spielen, sind weiße Blutzellen, die durch den Körper patrouillieren und infiziertes Gewebe sowie die meisten gefährlichen Krankheitserreger eliminieren können. Trotzdem sind diese Zellen keine Einzelkämpferinnen, denn sie arbeiten effektiv im Kollektiv zusammen. „Sobald ein Infektionserreger entdeckt ist, sendet der erste Neutrophile, der den Ort des Geschehens erreicht, ein chemisches Signal aus, um andere Zellen zu alarmieren“, erklärt Tim Lämmermann(öffnet in neuem Fenster), Forscher am Max-Planck-Institut für Immunbiologie und Epigenetik(öffnet in neuem Fenster), Deutschland. Wie Lämmermann erklärt, bilden die herbeieilenden Zellen auf dieses Signal hin einen Cluster, sodass der Infektionserreger von einem todbringender Schwarm angegriffen wird. Signal zur Einstellung des Angriffs „Theoretisch würde das Signal immer mehr Neutrophile anlocken, die schließlich auch das Gewebe schädigen, dass eigentlich verteidigt werden sollte“, fährt Lämmermann fort. Finanziert durch den Europäischen Forschungsrat(öffnet in neuem Fenster) untersuchten Lämmermann und sein Forschungsteam im Projekt IMMUNE CELL SWARMS biologische Grundlagen des Schwarmverhaltens Neutrophiler, aber auch, wie ein Angriff beendet wird.
(Molekulares) Abbremssignal
Mit einem speziellen mikroskopischen Verfahren konnten Neutrophile in Lebendgewebe in Echtzeit sichtbar gemacht werden, was nun deren integrierte Stoppfunktion enthüllte. So wird die Schwarmreaktion der Neutrophilen durch einen molekularen Prozess abgebremst: Sobald das chemische Signal einen Grenzwert erreicht hat, wird das Schwarmverhalten eingestellt. „Das Prinzip dabei ist, dass der Schwarm erspüren kann, wenn er die erforderliche Größe erreicht hat, weil es dann zur Unempfindlichkeit gegenüber den eigenen Signale kommt, die die Schwarmreaktion anfangs auslösten“, erklärt Lämmermann. „Wenn das passiert, eilen keine weiteren Neutrophilen herbei, da der Infektionserreger nun wirksam in Schach gehalten werden kann.“ Im nächsten Schritt entdeckte das Team mit GRK2 sogar genau das Protein, das dieses Abbremsen vermittelt: die G-Protein-gekoppelte Rezeptorkinase 2. „Es bewirkt, dass Neutrophile unempfindlich für das Signal ‚Angriff‘ werden, und zwar dann, wenn die maximal notwendige Truppenstärke erreicht ist“, so Lämmermann. Überraschend sei dieser Befund durchaus, wie er weiter ausführt, da man bislang davon ausging, dass die externen Signale, die die Neutrophilenaktivität stoppen, aus dem Gewebe selbst stammen. „Unsere Forschung belegt nun das Gegenteil“, sagt er. „Da Neutrophile die Fähigkeit zur Selbstregulation haben, wird im Kampf gegen Eindringlinge ein optimales Gleichgewicht zwischen Identifizierungs- und Zerstörungsphase hergestellt.“
Unerwartete Ergebnisse – neue Möglichkeiten
Das Projekt IMMUNE CELL SWARMS enthüllte einen wichtigen biologischen Aspekt von Neutrophilen, der den Wissensstand zur immunologischen Abwehr bakterieller Infektionen erweitert. „Die überraschenden Erkenntnisse darüber, wie Immunzellen Pathogene identifizieren und ausschalten, könnten den Weg für neue Therapien ebnen“, schließt Lämmermann. „Zudem bietet unsere Arbeit auch neue Forschungsansätze zum kollektiven Verhalten anderer Zellverbände.“ Lämmermann und sein Team untersuchen derzeit, inwieweit Krankheiten wie Diabetes und bakterielle Infektionen diese wichtige Fähigkeit der Selbstregulation bei Neutrophilen beeinflussen bzw. stören.