Descifrar el papel de los receptores nicotínicos en el cáncer de próstata y colon
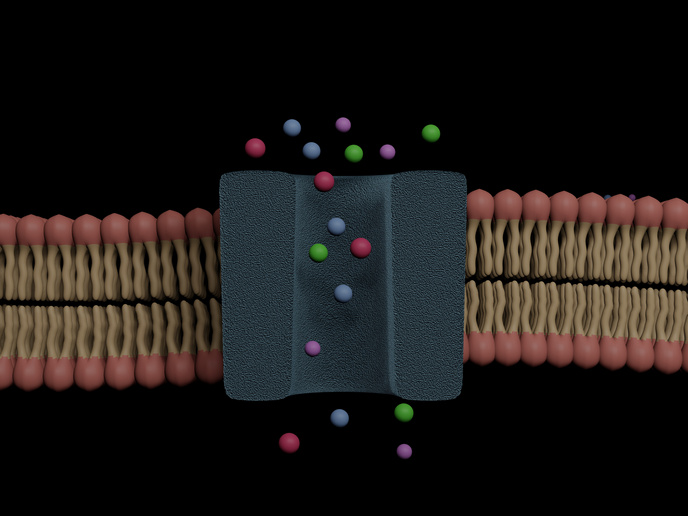
Los receptores nicotínicos de la acetilcolina(se abrirá en una nueva ventana) (nAChR) son canales iónicos transmembrana que se activan por el neurotransmisor acetilcolina o el fármaco nicotina. Constan de cinco subunidades codificadas por dieciséis genes diferentes, por lo que tienen propiedades y funciones diversas. Aunque los nAChR se expresan ampliamente en todo el sistema nervioso periférico y central, también se encuentran en todo el organismo. Además de sus propiedades ionotrópicas bien descritas, estos receptores también activan varias vías de señalización intracelular en las neuronas y otros tipos de células. Está claro que fumar tabaco se correlaciona con varios tipos de cáncer, ya que la nicotina y las nitrosaminas derivadas del tabaco activan los nAChR, lo que contribuye a la progresión del cáncer y a la resistencia a la quimioterapia. En el cáncer de pulmón, se sabe que la exposición a la nicotina por la interacción con los nAChR aumenta la proliferación celular, la transición epitelial a mesenquimal y la invasión celular. Sin embargo, las contribuciones específicas de los nAChR a la fisiopatología de los cánceres de próstata y colon siguen sin ser exploradas.
Expresión de los nAChR en el cáncer
Realizado con el apoyo de las Acciones Marie Skłodowska-Curie(se abrirá en una nueva ventana) (MSCA), el equipo del proyecto nAChRs-CRC-PCa-IF-RI tenía como objetivo identificar y caracterizar los nAChR específicos implicados en los cánceres de próstata y colon. «Queríamos entender el papel de estos receptores en los procesos celulares como la migración, la proliferación y la invasión», explica Maria Maldifassi, beneficiaria de una beca de investigación de las MSCA. Los investigadores estudiaron los niveles de los nAChR en las células de cáncer de mama, colon y próstata y observaron patrones de expresión distintos. En particular, la expresión de la subunidad nicotínica α5(se abrirá en una nueva ventana) resultó ser crucial para la proliferación y migración inducidas por la nicotina. La regulación a la baja de la α5 perjudicó la migración de las células cancerosas al reducir la expresión de los marcadores de transición epitelial mesenquimal (TEM) y las proteínas reguladoras inmunitarias, típicamente promovidas por la nicotina. Otro descubrimiento fundamental fue el impacto de la variante genética de la subunidad α5 (polimorfismo D398N), vinculada a la dependencia de la nicotina en el cáncer de pulmón. Este polimorfismo provocó un aumento basal de la proliferación y la migración en las células de cáncer de próstata. En conjunto, estos resultados sugieren que la proliferación y la migración de las células cancerosas inducidas por la nicotina se producen a través de la α5, lo que la convierte en una posible diana terapéutica.
Modelos de cáncer en 3D
En los proyectos se utilizaron con éxito los cultivos en 3D(se abrirá en una nueva ventana) para evaluar los efectos de la nicotina sobre la viabilidad de las células cancerosas y la expresión de los marcadores. Los resultados indicaron que la activación nicotínica de los nAChR podía modificar la viabilidad y aumentar la regulación de los marcadores del cáncer de pulmón, pero no en las esferas del cáncer de próstata. En comparación con los cultivos convencionales en 2D, estos modelos de cáncer en 3D se asemejan más al entorno fisiológico para el estudio de la invasión y migración de las células inmunitarias en tumores sólidos.
Perspectivas de futuro
«En conjunto, en el proyecto se mejoró nuestra comprensión de los efectos promotores de tumores de la nicotina más allá del cáncer de pulmón. Se demostró que el consumo de nicotina también está asociado con el cáncer de próstata, el cáncer colorrectal y el cáncer de mama, lo que destaca el potencial de la subunidad α5 para servir de diana terapéutica», enfatiza Maldifassi. De cara al futuro, el equipo de investigación tiene previsto establecer modelos de cáncer en 3D, como el pez cebra y los xenoinjertos derivados de pacientes, y emplear métodos farmacológicos para seguir investigando el papel de la subunidad α5 en los mecanismos prooncogénicos del cáncer. Además, el desarrollo de modelos de cáncer en 3D será decisivo para explorar las funciones de otros canales iónicos en la progresión del cáncer.