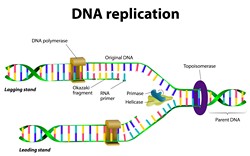
La reprise de la réplication réussie de l'ADN sur les fourches calées
Le calage aux fourches de réplication causé par une interférence avec la progression, la stabilité et le redémarrage peuvent provoquer le cancer. Smc5-Smc6 est un complexe de plusieurs sous-unités qui est responsable de la progression des fourches de réplication via l'ADN endommagé et est recruté pour les fourches qui s'effondrent. Le projet CHROMOSOME STABILITY (Coordination of DNA replication and DNA repair at single-forks: the role of the Smc5-Smc6 complex in replication fork stalling and resumption) a identifié des sites de modification post-translationnelle par une partie de la machine Smc5-Smc6. Les chercheurs ont examiné en particulier le petit modificateur similaire à l'ubiquitine SUMO qui dépend d'une sous-unité de Smc5-Smc6, Nse2. SUMO est impliqué dans la modification post-translationnelle. Les objectifs SUMO identifiés par l'équipe comprennent Scc1. Les résultats de la recherche montrent que Scc1 SUMOylation par Nse2 est nécessaire pour la réparation d'une rupture d'ADN double brin. Un autre objectif Sgs1 est important pour son rôle dans un cancer humain appelé syndrome de Bloom. Les données ont confirmé que Sgs1 est impliqué dans la fixation des intermédiaires de recombinaison aux fourches endommagées ou calées. Contre toute attente, les chercheurs ont également découvert un changement dans le statut de bobinage de l'ADN aux fourches compromises. Comme l'absence de réparation et de redémarrage des erreurs de réplication aux fourches peut conduire à différents cancers, la connaissance des machines moléculaires pourrait conduire à de nouveaux objectifs thérapeutiques. Une approche personnalisée à ce niveau promet de réduire considérablement les effets secondaires très désagréables et d'augmenter l'efficacité thérapeutique.