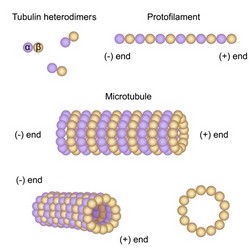
La base molecolare della polarità cellulare
Le cellule hanno la capacità intrinseca di polarizzare la loro struttura e la loro funzione. Ciò significa che in seguito a uno spunto extracellulare esse distribuiscono in modo asimmetrico gli elementi del citoscheletro e del sistema membrana, dando origine al traffico di membrana polarizzato. Questa proprietà facilita molti processi biologici, tra cui lo sviluppo dei tessuti, la trasmissione neurale e le risposte immunitarie. Un ruolo centrale nella polarità cellulare è esercitato dal citoscheletro dei microtubuli. Evidenze crescenti indicano che gli eventi della membrana plasmatica, compresa l’attivazione dei recettori, la segnalazione dell’integrina e l’attivazione di alcuni fattori sono necessari per la stabilizzazione dei microtubuli, tuttavia il meccanismo regolatore di questo processo e della polarità restano ancora poco chiari. Il progetto CELL POLARITY (Role of microtubule polarity and polarized membrane traffic in directed cell migration), finanziato dall’UE, ha cercato di delineare questi meccanismi molecolari e di identificare i fattori centrali per il traffico diretto. A questo scopo, ha creato un sistema di fibroblasti a bordo ferita, impiegando metodi di imaging ad alta e altissima risoluzione per quantificare i cambiamenti subiti dai microtubuli dopo il knockdown di fattori specifici. I risultati indicano che due proteine di polarità evolutivamente conservate, Numb e Par3, svolgono ruoli opposti nella stabilizzazione dei microtubuli. L’adattatore endocitico Numb agisce come nuovo soppressore della stabilità dei microtubuli, mentre la proteina di polarità dello scaffold Par3 è necessaria per la stabilizzazione. Questa interazione Numb/Par3 potrebbe determinare in modo preciso la quantità di microtubuli stabili, regolando di conseguenza la velocità o la persistenza della migrazione cellulare diretta. Gli scienziati, inoltre, hanno espresso la Par3 fluorescente per visualizzare il suo comportamento spaziotemporale nella migrazione delle cellule, identificando due distinti gruppi di Par3, uno statico nei contatti tra cellule e uno dinamico sul bordo avanzato. L’identificazione del significato biologico del gruppo dinamico potrebbe aiutare a delinearne la similarità con il flusso retrogrado di actina e la stabilizzazione dei microtubuli. Gli scienziati, inoltre, hanno impiegato nuovi metodi di imaging ad altissima risoluzione basati su fluorescenza come la microscopia a illuminazione strutturata, la microscopia a deplezione di emissione stimolata e la microscopia di ricostruzione ottica stocastica diretta, ottenendo una migliore risoluzione rispetto ai metodi convenzionali di analisi dell’organizzazione spaziotemporale delle proteine e degli organuli subcellulari nella polarità cellulare. Nel complesso, lo studio CELL POLARITY ha individuato nuovi legami meccanicistici tra l’endocitosi delle integrine, lo switching dei fosfoinositidi e la stabilità dei microtubuli. Considerato il ruolo di molti di questi fattori in malattie come il cancro e le disfunzioni neurologiche, i risultati del progetto offrono nuovi obiettivi per l’intervento terapeutico.