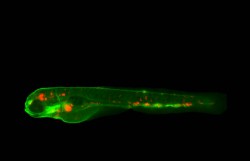
Zebrafische im Kampf gegen Tuberkulose
Gegenwärtig wird Tuberkulose mit chemotherapeutischen Medikamenten behandelt. Um Arzneimittelresistenzen gegenzusteuern, wird nach neuen therapeutischen Ansätzen gesucht, die z. B. gezielt auf die Wirtszellen ausgerichtet sind. Um derzeitige therapeutische Strategien gegen Tuberkulose zu verbessern, soll nun intensiver an der angeborenen Immunantwort und den Mechanismen geforscht werden, mit denen der Krankheitserreger die Wirtsabwehr umgeht. In der Forschung gilt Autophagie inzwischen als entscheidender Abwehrmechanismus des Wirts, der den Tuberkuloseerreger schwächt und ihm das Überleben in der Wirtszelle erschwert. Durch einen autophagischen Prozess werden die Bakterien gezielt eliminiert, und Autophagie steuert offenbar auch Entzündungsreaktionen. Zur Interaktion zwischen Entzündung und Autophagie bei der Abwehr der Tuberkuloseerreger durch den Wirt ist allerdings noch zu wenig bekannt. So forschte das EU-finanzierte Projekt Inflammafish(öffnet in neuem Fenster) am etablierten Zebrafischmodell für Tuberkulose zu Entzündung und Autophagie: zwei für die Tuberkulose-Pathogenese so wichtige Prozesse. Zur Rolle von Autophagie und Entzündung bei der Infektion „Das Projekt Inflammafish sollte die Mechanismen der Wirtsabwehr gegen Tuberkulose genauer erforschen und neue therapeutische Zielstrukturen finden“, erklärt Projektkoordinatorin Prof. Annemarie Meijer. Die Forschergruppe führte ihre Untersuchungen am Zebrafischmodell durch, da sich die Prozesse dort besonders gut in vivo beobachten lassen. Frühere Forschungen der Gruppe hatten enthüllt, dass der Autophagiemodulator DRAM1 (DNA damage-regulated autophagy modulator) das Zebrafischmodell vor Tuberkulose schützen konnte. Nach Meinung der Wissenschaftler wird dieser wichtige Autophagieregulator auch mit Entzündungen assoziiert, da er stark die Expression von Interleukin-1beta beeinflusst. Interessant dabei war, dass es offenbar ausreicht, einen dieser Signalwege zu unterbrechen, um den Infektionsverlauf bei Tuberkulose zu hemmen. Ist diese autophagische Reaktion des Wirts gestört, können sich die Bakterien in seinen Zellen ungehindert vermehren. Vor allem beobachteten die Wissenschaftler, dass der Erreger die Entzündungsreaktion zu seinem eigenen Vorteil so verändern kann, dass proinflammatorische Prozesse das Absterben der infizierten Zellen induzieren und sich die Infektion rascher ausbreitet. Demzufolge könnte durch Manipulation eines der Schlüsselproteine des inflammatorischen Signalwegs das Infektionsgeschehen gestoppt werden. Wege zu neuen Therapien „Zusammenfassend zeigen unsere Ergebnisse, dass die Aktivierung von Entzündungsreaktion und Autophagie Voraussetzung für eine effektive Abwehr des Tuberkuloseerregers ist“, erklärt die Marie-Curie-Stipendiatin und Forscherungsleiterin Dr. Marie Varela. Derzeit wird nun die Interaktion dieser Signalwege mit unterschiedlichen Zelltodmechanismen untersucht, um zu klären, was mit infizierten Makrophagen geschieht und wie der Infektionsverlauf beeinflusst wird. Schließlich will die Forschergruppe von Inflammafish genomweite Effekte der Autophagiemodulation auf die Entzündungsreaktion untersuchen, um neue therapeutische Zielstrukturen gegen Tuberkulose zu finden. Schwerpunkt künftiger Forschungen wird daher die Entwicklung neuer Strategien gegen Tuberkulose mit chemischen Modulatoren der Autophagie- und Entzündungswege sein. Weitere Erkenntnisse zur möglichen Manipulation regulatorischer Signalwege beim Wirt können neue therapeutische Optionen gegen Tuberkulose und andere Krankheiten mit ähnlichen Merkmalen aufzeigen. Prof. Meijer wünscht sich, dass „künftige Tuberkulosemedikamente in die Interaktion zwischen Wirt und Pathogen eingreifen, um des Resistenzproblems bei derzeitigen Arzneimitteln Herr zu werden“.