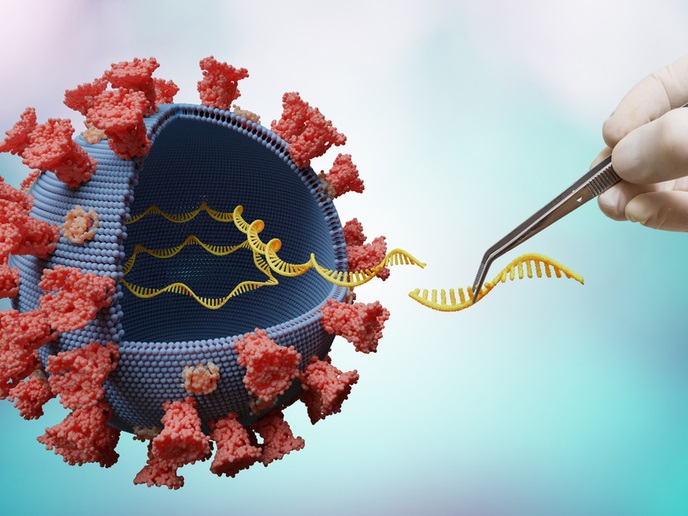
Wiedza na temat wirusowych modyfikacji RNA kluczem do produkcji leków przeciwwirusowych
Modyfikacje bazujące na cząsteczkach RNA to niezmienne ewolucyjnie zjawisko obserwowane zarówno u komórek eukariotycznych, jak i prokariotycznych, co może wskazywać na ich istotne funkcje. Potranskrypcyjna modyfikacja RNA, N6-metyloadenozyna(odnośnik otworzy się w nowym oknie) (m6A), to najpowszechniej występująca modyfikacja w komórkach eukariotycznych, która przyspiesza metabolizm i translację mRNA. Działa ona na zasadzie sygnału naprowadzającego, który wykrywany jest przez konkretne białka w cytoplazmie i który kieruje działaniem RNA podczas różnych procesów biologicznych.
Mapowanie modyfikacji m6A na wirusowym RNA
O obecności modyfikacji m6A na wirusowych RNA wiedziano od ponad 30 lat, ale brak odpowiedniej technologii uniemożliwiał jej dokładniejsze zbadanie. Celem zespołu projektu IAV-m6A było zmapowanie modyfikacji m6A na genomie wirusa grypy typu A(odnośnik otworzy się w nowym oknie) (IAV) i poznanie ich funkcji. Badania zostały zrealizowane dzięki wsparciu uzyskanemu w ramach programu „Maria Skłodowska-Curie”. „Badanie miało odkryć rolę modyfikacji m6A w replikacji wirusa i wyjaśnić, jak utrata tych modyfikacji wpłynęłaby na patogenezę wirusa”, mówi David Courtney, stypendysta programu „Maria Skłodowska-Curie”. Wykorzystując metodę opartą na przeciwciałach, Courtney rozpoznał lokalizację modyfikacji m6A na wirusowym RNA, a następnie przeprowadził mutację genomu IAV, aby zapobiec wiązaniu m6A w tych miejscach. Kolejnym krokiem było wykonanie charakterystyki in vitro i in vivo tych zmutowanych wirusów, która potwierdziła, że modyfikacje m6A wspierają replikację IAV. W oparciu o spektrometrię mas naukowiec zbadał dodatkowe modyfikacje RNA, takie jak 5-metylocytozyna (m5C), i odkrył, że wraz z m6A są one wzbogacone na genomach wirusów RNA w porównaniu do komórkowych mRNA. „Odkrycie znacznego wzbogacenia modyfikacji na genomach wirusów RNA, takich jak wirus grypy typu A i wirus HIV-1, było jednym z najważniejszych ustaleń projektu i prawdopodobnie odzwierciedla ewolucję wirusów”, zauważa Courtney. Co ważne, modyfikacje te sprzyjają cyklowi replikacyjnemu wirusa i produkcji białek. Replikacja IAV przebiegała znacznie wolniej w komórkach pozbawionych METTL3(odnośnik otworzy się w nowym oknie) – kluczowego białka, które składuje modyfikacje m6A na matrycy RNA. Komórki te produkowały także mniej IAV po zakażeniu, podkreślając istotną rolę m6A w regulacji RNA wirusa grypy typu A. Ustalenia naukowców zostały potwierdzone przez badania komórek charakteryzujących się nadekspresją białek YTHDF1 i YTHDF2, które wykrywają modyfikacje m6A charakteryzujące się wzrostem poziomu stężenia RNA i białka.
Prognozy na przyszłość
Chociaż badania wirusologiczne przeprowadzone w ramach projektu IAV-m6A nie miały znaczenia klinicznego, dostarczyły cennej wiedzy na temat ewolucji wirusa i jego cyklu życia, która może być wykorzystana w innych badaniach. Rozpoznanie kluczowych białek lub modyfikacji zaangażowanych w replikację wirusa może zaowocować powstaniem nowych cząsteczek przeciwwirusowych, które ograniczyłyby rozprzestrzenianie się wirusów. Ponadto ustalenia projektu mogą pomóc w zwiększeniu produkcji białek IAV, co umożliwiłoby zwiększenie produkcji szczepionek i zaspokojenie zapotrzebowania na nie. David Courtney otrzymał grant na rozpoczęcie badań, ERC Starting Grant, który pomoże mu zebrać własny zespół naukowców na Queen’s University Belfast (Zjednoczone Królestwo). Celem zespołu będzie prowadzenie dalszych badań, które pomogą wyjaśnić, jak wirus grypy typu A wykorzystuje różne modyfikacje RNA podczas cyklu replikacyjnego. Zbadane zostaną także inne mechanizmy potranskrypcyjnej regulacji RNA wirusa grypy typu A.