Bionisches menschliches Mikrogewebe für die Wirkstoffforschung
Ein Hauptgrund für die hohe Ausfallrate in der Arzneimittelforschung ist, dass sich menschliche Reaktionen an Tiermodellen aufgrund physiologischer und genetischer Unterschiede nicht genau vorhersagen lassen. Die Entwicklungskosten für ein Medikament liegen daher bei durchschnittlich mehr als 2,6 Milliarden USD(öffnet in neuem Fenster). Diese Vorhersagbarkeit soll nun eine mikrofluidische Plattform verbessern, die die menschliche Physiologie simuliert und – eingebettet in menschliches Mikrogewebe – dessen genetische Eigenschaften und Stoffwechselprozesse verdeutlicht. Das vom Europäischen Forschungsrat(öffnet in neuem Fenster) finanzierte Projekt OCLD ging nun einen Schritt weiter und stattete das Mikrogewebe mit integrierten elektronischen Sensoren aus. „Über unsere Plattform DynamiX konnten wir mit menschlichen Organen ‚kommunizieren‘ und so Daten zu Krankheitsprozessen wie Nierenschäden oder Virusinfektionen generieren, was wiederum die Wirkstoffforschung verbessern kann“, erklärt Projektkoordinator Yaakov Nahmias(öffnet in neuem Fenster) von der Hebräischen Universität Jerusalem(öffnet in neuem Fenster), die das Projekt koordinierte. Da DynamiX kürzlich das Exzellenzsiegel der Europäischen Kommission erhielt, kann es nun durch das Spin-off-Unternehmen Tissue Dynamics(öffnet in neuem Fenster) auf den Markteintritt vorbereitet werden.
Miniaturmodelle für bessere Vorhersagbarkeit
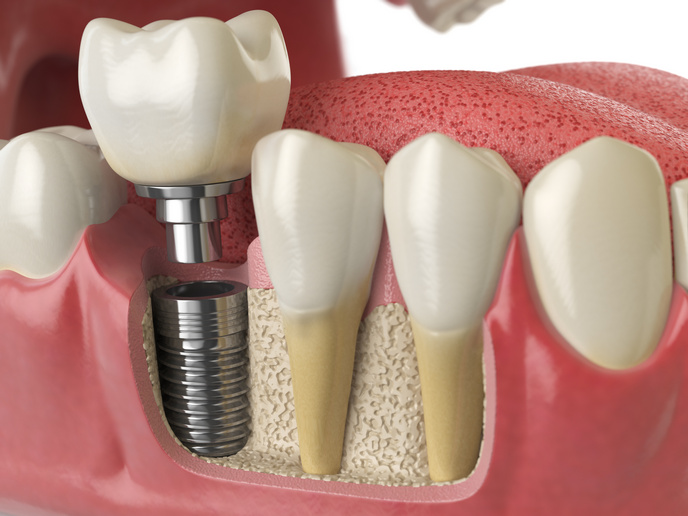
Vorläufer von OCLD war das Projekt HeMiBio, das 2012 für das Unternehmen L’Oréal erstmals Sensoren in Mikrogewebe integrierte. Mikrogewebe sind Miniaturmodelle menschlicher Organe. OCLD entnahm nun menschliche Zellen aus Leber, Niere und Lunge, bearbeitete sie mit gentechnischen Verfahren und züchtete sie außerhalb des Körpers. Die Zellen wurden mit Endothelzellen(öffnet in neuem Fenster) zusammengebracht, sodass sich Blutgefäße von etwa einem halben Millimeter Durchmesser bildeten, die in menschliches Gewebe einwuchsen. Diese Mikrogewebe funktionieren ähnlich wie im menschlichen Körper. In jedes Mikrogewebe sind ein bis vier Sauerstoffsensoren eingebettet, die etwa so breit sind wie ein menschliches Haar und mehrere Monate lang Daten zur Zellrespiration im Gewebe liefern. Die Gewebe werden auf einen mikrofluidischen Chip platziert, auf dem sich elektrochemische Sensoren befinden, die länger als einen Monat kontinuierlich den Verbrauch von Glukose, Laktat und Glutamin im Gewebe überwachen. Ein Softwareprogramm wertet dann die Signale der Plattform aus, und anhand der erstellten Computermodelle des Zellstoffwechsels können Störungen erkannt werden, die auf Krankheiten hinweisen. Auf diese Mikrogewebemodelle wurden nun verschiedene Medikamente gegeben. Am Lebermodell, das die Forschenden generierten, zeigte sich, dass das HIV-Medikament Stavudin(öffnet in neuem Fenster) durch unzureichende Lipidoxidation eine Fettlebererkrankung verursachen kann, was dem Ergebnis am Nagermodell entsprach. Anders als beim Tiermodell hingegen zeigte das Mikrogewebemodell, dass das Antiepileptikum Valproinsäure(öffnet in neuem Fenster) die Glukoseaufnahme erhöht und so eine Fettlebererkrankung verursachen kann, was im Leitartikel des Journals „Lab on a Chip“(öffnet in neuem Fenster) beschrieben wurde. Das Nierenmodell der Forschenden zeigte wiederum, dass das Krebsmedikament Cisplatin(öffnet in neuem Fenster) durch Lipidakkumulation Nierenschäden verursacht, statt wie das Nagermodell nahelegte, nur eine Erweiterung der Blutgefäße. Die im Leitartikel von „Science Translational Medicine“(öffnet in neuem Fenster) veröffentlichte Arbeit zeigte, dass sich Schäden durch Cisplatin verhindern lassen, wenn es mit Empagliflozin(öffnet in neuem Fenster) kombiniert wird. Die Kombination konnte sogar die schlimmsten Nebenwirkungen einer Chemotherapie verhindern. „Dies könnte nicht nur Chemotherapien sicherer und wirksamer machen, sondern auch auf andere Bereiche anwendbar sein. Während der COVID-19-Pandemie identifizierte DynamiX einen ähnlichen Lipidakkumulationsprozess bei menschlichen Lungenzellen. Unsere Methoden lieferten klinische Daten für Fenofibrat(öffnet in neuem Fenster) als potenziellen antiviralen Wirkstoff, der Menschen künftig vor dem Corona-Virus schützen könnte“, sagt Nahmias. Das Ergebnis wird derzeit in einer vom Pharmaunternehmen Abbott finanzierten klinischen Phase-3-Studie geprüft.
Neues Paradigma für die Wirkstoffforschung
DynamiX lieferte ein hervorragendes Instrument für die Wirkstoffforschung, das bereits vor dem Beginn klinischer Studien oder einer Zulassung Sicherheitsrisiken aufzeigen kann. Da es sowohl lang- als auch kurzfristige Toxizitätsrisiken erkennt, vereinfacht es auch die Dosisfindung (Mindest- und Maximaldosis) für Wirkstoffe vor klinischen Studien. Tissue Dynamics wirbt nun 10 Millionen USD für klinische Studien zu einem neuen Medikament gegen Fettlebererkrankung ein und strebt die Finanzierung mehrerer klinischer onkologischer Studien an, um Krebsmedikamente sicherer zu machen.