Une première pour le traitement du cancer du pancréas chez les modèles murins
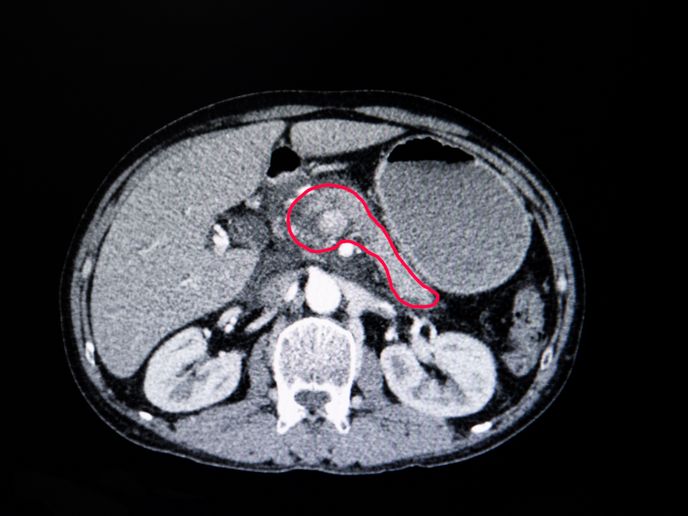
Bien qu’il s’agisse de l’une des principales causes de décès dans le monde(s’ouvre dans une nouvelle fenêtre), la plupart des cancers peuvent être traités s’ils sont détectés suffisamment tôt. Les cancers du pancréas et du poumon se distinguent toutefois par leur faible taux de survie. «Ces cancers ne provoquent généralement des symptômes qu’à un stade avancé, ce qui rend très difficile l’ablation chirurgicale de la tumeur ou d’autres traitements», explique Mariano Barbacid, coordinateur du projet THERACAN, qui a été financé par le Conseil européen de la recherche(s’ouvre dans une nouvelle fenêtre). Comme ces deux cancers sont dus à des mutations génétiques spécifiques, connues sous le nom d’oncogènes KRAS(s’ouvre dans une nouvelle fenêtre), THERACAN a utilisé des modèles de tumeurs de souris génétiquement modifiées (GEM pour «genetically engineered mouse») (in vivo et in vitro) pour étudier les mécanismes moléculaires sous-jacents responsables. Le projet a identifié de nouvelles cibles thérapeutiques impliquées dans la signalisation oncogénique KRAS, démontrant que les cellules tumorales régressaient dans les deux cancers après l’élimination de ces cibles par manipulation génétique.
Le rôle des oncogènes KRAS
Selon Mariano Barbacid, les oncogènes KRAS sont responsables d’environ un quart de toutes les tumeurs humaines solides, dont 25 % des adénocarcinomes(s’ouvre dans une nouvelle fenêtre) (cancers qui se développent dans les glandes tapissant les organes) du poumon et plus de 90 % des tumeurs du pancréas. Bien qu’elles aient été parmi les premiers oncogènes humains découverts en 1982, on pensait qu’en raison de leur taille et de leur forme, les oncoprotéines KRAS ne pouvaient pas être ciblées par des médicaments. Ce n’est que récemment que les sociétés pharmaceutiques ont pu concevoir des médicaments inhibiteurs sélectifs de l’oncogène KRAS. Pourtant, comme l’explique Mariano Barbacid, les options restent limitées. «Jusqu’à présent, la Food and Drug Administration(s’ouvre dans une nouvelle fenêtre) des États-Unis n’a approuvé que deux médicaments inhibiteurs pour l’une des formes mutées du gène KRAS. Malheureusement, les résultats cliniques ont été modestes, la moitié seulement des patients atteints d’un cancer du poumon ayant vu leur tumeur régresser. Le taux de survie du cancer du poumon à deux ans était le même que celui observé avec les anciens traitements cytotoxiques. Les résultats étaient encore moins impressionnants pour les tumeurs du pancréas, d’où l’urgence de développer de nouveaux inhibiteurs.»
Des souris génétiquement modifiées
Les modèles de tumeurs de GEM ont permis à l’équipe de supprimer les cibles protéiques de l’oncogène soupçonnées de jouer un rôle important dans le développement des tumeurs. L’équipe a démontré que l’élimination de RAF1, une protéine impliquée dans la signalisation KRAS (qui contrôle la prolifération cellulaire, y compris dans les cancers), entraînait la régression de deux tiers des tumeurs pulmonaires mutantes KRAS. Plus important encore, l’élimination de RAF1 et du récepteur EGF (qui fait également partie du processus de signalisation) entraînait la régression complète d’un pourcentage élevé d’adénocarcinomes canalaires du pancréas. Comme il n’existe pas d’inhibiteurs sélectifs de RAF1 pouvant être utilisés pour valider les résultats, l’équipe a utilisé des modèles de xénogreffes de tumeurs dérivées de patients(s’ouvre dans une nouvelle fenêtre) (des cellules tumorales humaines cultivées dans des souris). Le médicament anticancéreux Gefitinib(s’ouvre dans une nouvelle fenêtre) a été utilisé comme inhibiteur de l’EGFR. «Il s’agit du premier rapport(s’ouvre dans une nouvelle fenêtre) sur la régression complète de ce type de tumeur dans un modèle expérimental», fait remarquer Mariano Barbacid. «Même si nous l’avons démontré dans un modèle animal, qui n’est donc pas directement comparable au modèle humain, observer la disparition complète des tumeurs du pancréas a été extrêmement passionnant.»
Accélérer la mise à disposition de nouvelles thérapies
Étant donné que les traitements pharmaceutiques mettent généralement de nombreuses années à passer des essais cliniques à la pratique médicale, des projets tels que THERACAN jouent un rôle essentiel dans l’identification de cibles prometteuses pour l’intervention thérapeutique. «Notre travail aide l’industrie pharmaceutique à concentrer ses ressources, accélérant ainsi le temps nécessaire au développement de médicaments inhibiteurs sélectifs, ce qui profite en fin de compte aux patients atteints de cancer», conclut Mariano Barbacid. L’équipe poursuit actuellement un projet financé par l’UE visant à développer de nouvelles stratégies génétiques pour faire régresser complètement toutes les tumeurs pulmonaires et pancréatiques mutantes KRAS dans les modèles de GEM.