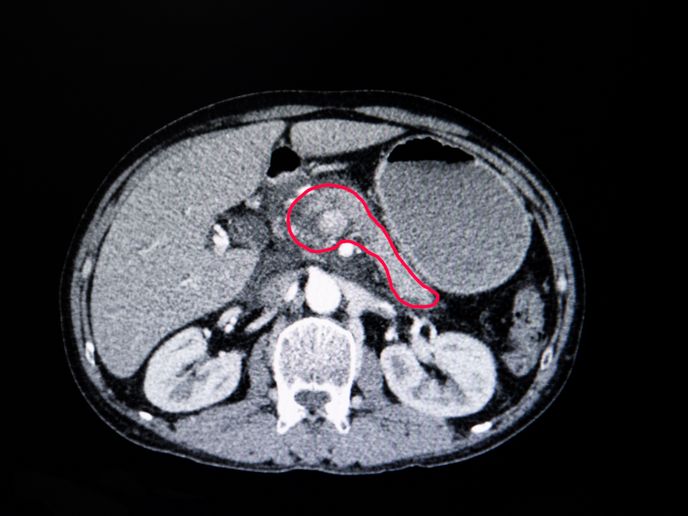
Erster Behandlungserfolg von Bauchspeicheldrüsenkrebs bei Mausmodellen
Obwohl Krebserkrankungen zu den weltweit häufigsten Todesursachen(öffnet in neuem Fenster) zählen, sind die meisten Krebsarten bei rechtzeitiger Diagnose behandelbar. Bei Bauchspeicheldrüsen- und Lungenkrebs sind die Überlebensraten jedoch niedrig. „Hier zeigen sich normalerweise erst im weit fortgeschrittenen Stadium Symptome, was eine chirurgische Entfernung oder andere Therapien sehr schwierig macht“, sagt Mariano Barbacid, Koordinator des über den Europäischen Forschungsrat(öffnet in neuem Fenster) finanzierten Projekts THERACAN. Da beiden Krebsarten spezifische genetische Mutationen zugrunde liegen, sogenannte KRAS-Onkogene(öffnet in neuem Fenster), erforschte THERACAN in vivo und in vitro ursächliche molekulare Mechanismen an gentechnisch veränderten Maus-Tumormodellen (genetically engineered mouse, GEM). Identifiziert wurden neue therapeutische Zielstrukturen im Zusammenhang mit der Signalübertragung von KRAS-Onkogenen, nach deren Eliminierung durch genetische Manipulation bei beiden Krebsarten die Zahl der Tumorzellen zurückging.
Zur Rolle von KRAS-Onkogenen
Laut Barbacid geht etwa ein Viertel aller soliden menschlichen Tumore auf KRAS-Onkogene zurück, u. a. 25 % aller Adenokarzinome(öffnet in neuem Fenster) der Lunge (ausgehend von malignen Veränderungen im Drüsengewebe der Epithelschicht von Organen), sowie mehr als 90 % aller Pankreastumore. Obwohl KRAS-Onkoproteine bereits 1982 als eine der ersten menschlichen Onkogene entdeckt wurden, galt bislang, dass sie aufgrund ihrer Größe und Form nicht medikamentös behandelt werden können. Erst kürzlich konnten Pharmaunternehmen selektive Inhibitoren für KRAS-Onkogene entwickeln, deren Möglichkeiten Barbacid zufolge aber begrenzt sind. „Bisher hat die Behörde für Lebens- und Arzneimittel FDA(öffnet in neuem Fenster) in den Vereinigten Staaten lediglich zwei Inhibitoren für eine der KRAS-Mutationen zugelassen. Allerdings blieb der klinische Erfolg überschaubar, da sich der Tumor nur bei der Hälfte der Lungenkrebskranken zurückbildete. Auch die Zwei-Jahres-Überlebensrate war nicht höher als bei herkömmlichen zytotoxischen Medikamenten. Bauchspeicheldrüsentumore schnitten sogar noch schlechter ab, was die Notwendigkeit neuer inhibitorischer Wirkstoffe verdeutlicht.“
Gentechnisch veränderte Mäuse
An gentechnisch veränderten Mausmodellen gelang es, die Onkogen-Proteinziele zu eliminieren, die offenbar eine wichtige Rolle bei der Tumorentwicklung spielen. Die Eliminierung des Proteins RAF1, das an der KRAS-Signalübertragung beteiligt ist (die wiederum die Zellproliferation auch bei Tumoren steuert), führte bei zwei Dritteln der auf KRAS-Mutationen zurückgehenden Lungentumoren zur Rückbildung, wie das Forschungsteam belegte. Vor allem aber erbrachte die Eliminierung sowohl von RAF1 als auch des EGF-Rezeptors (ebenfalls Teil des Signalprozesses) beim Großteil duktaler Pankreas-Adenokarzinome eine vollständige Regression. Da noch keine selektiven RAF1-Inhibitoren zur Validierung der Ergebnisse existieren, wurde dies an Tumormodellen mit patienteneigenen Xenotransplantaten(öffnet in neuem Fenster) (in Mäusen gezüchtete menschliche Tumorzellen) durchgeführt. Dabei kam das Krebsmedikament Geftinib(öffnet in neuem Fenster) als EGFR-Hemmer zum Einsatz. „Dies war der erste Bericht(öffnet in neuem Fenster) einer vollständigen Rückbildung dieses Tumortyps in allen experimentellen Modellen“, erläutert Barbacid. „Obwohl wir dies nur am Tiermodell zeigen konnten – was nie direkt mit dem Menschen vergleichbar ist – war das vollständige Verschwinden des Pankreastumors höchst bedeutsam.“
Beschleunigung der Verfügbarkeit neuer Therapien
Da die Entwicklung pharmazeutischer Wirkstoffe von der klinischen Phase bis zur klinischen Umsetzung in der Regel viele Jahre dauert, tragen Projekte wie THERACAN maßgeblich zur Identifizierung vielversprechender Ziele für therapeutische Interventionen bei. „Dank unserer Arbeit können Pharmaunternehmen Ressourcen bündeln und die Entwicklungszeit für selektive Inhibitoren verkürzen, was letztlich Betroffenen zugute kommt“, schließt Barbacid. Nun will das Team in einem EU-finanzierten Projekt an Mausmodellen neue genetische Strategien zur vollständigen Rückbildung aller Lungen- und Pankreastumore erforschen, die auf KRAS-Mutationen zurückgehen.