È il rame il metallo incriminato nella malattia di Alzheimer
La malattia di Alzheimer (AD) è stata descritta ufficialmente per la prima volta nel 1906 e, dopo alcuni anni, la classificazione di «malattia di Alzheimer» è stata inserita in un manuale di psichiatria. Nonostante da allora siano trascorsi più di cento anni di dati e ricerche a livello clinico, rimangono molti interrogativi aperti e, tra questi, uno rilevante a cui è stata fornita una risposta con il progetto aLzINK, finanziato dal Consiglio europeo della ricerca (CER) dell’UE, che ha indicato la strada verso un bersaglio importante per i farmaci candidati che potrebbero evitare lo sviluppo di questa malattia neurologica degenerativa devastante.
I metalli non sono tutti uguali
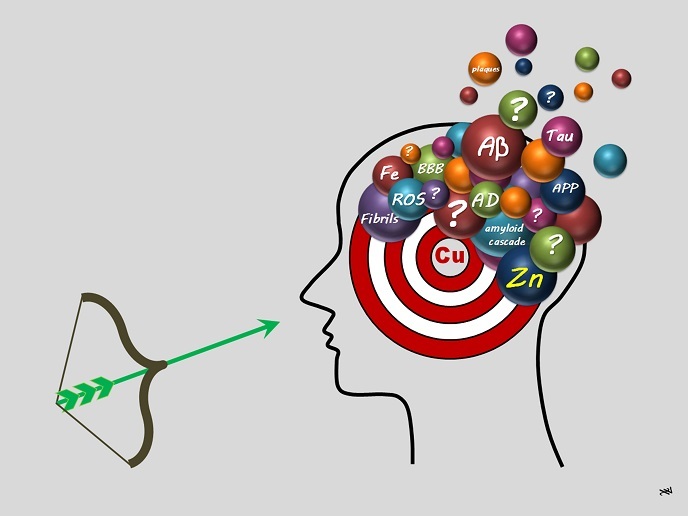
Negli ultimi 30 anni, l’ipotesi della cascata amiloide(si apre in una nuova finestra) ha rappresentato un aspetto centrale della ricerca sull’AD. Questa ipotesi suggerisce che l’aggregazione di peptidi β-amiloidi(si apre in una nuova finestra) (Aβ) (in cui i peptidi sono due o più amminoacidi legati in una catena) costituisce un evento precoce e il primo evento principale. Il secondo evento consiste nella formazione di specie reattive dell’ossigeno (ROS, Reactive Oxygen Species)(si apre in una nuova finestra) correlate allo stress ossidativo(si apre in una nuova finestra). Nello stadio finale, i peptidi auto-assemblati sono riuniti nelle cosiddette placche senili, elementi caratteristici della malattia. L’omeostasi dei metalli (che mantiene il corretto equilibrio di metalli necessario per le funzionalità fisiologiche), in particolare del rame (Cu) e dello zinco (Zn), è stata collegata a tutti e tre gli stadi. Christelle Hureau-Sabater, beneficiaria del CER, spiega: «Il Cu è reperibile in due stati di ossidazione, Cu+ e Cu2+. Mentre il rame può innescare la formazione delle ROS, lo zinco è inerte e non può. Entrambi gli ioni possono legarsi ai peptidi Aβ, ma con modalità differenti in quanto essi modulano l’aggregazione dei peptidi Aβ in modo diverso. Una strategia terapeutica si basa sulla rimozione del legame degli ioni metallici ai peptidi Aβ. Abbiamo ipotizzato che il rame debba essere rimosso selettivamente, il che rende più difficoltosa la progettazione di molecole terapeutiche/farmaci candidati (chiamati ligandi o agenti chelanti)». Il progetto aLzINK ha definito lo sviluppo di apposite linee guida.
Superare le sfide, centrare il bersaglio
Il peptide Aβ è una proteina corta intrinsecamente disordinata di circa 40 amminoacidi che deriva da una proteina di membrana più lunga. La sua flessibilità e la mancanza di una struttura 3D preformata rendono difficile individuare dove e in che modo il rame e lo zinco si legano al peptide. In base alle affermazioni di Hureau-Sabater, «abbiamo superato questo problema utilizzando molte tecniche complementari, tra cui la sofisticata spettroscopia di assorbimento di raggi X(si apre in una nuova finestra) o XAS». La XAS è ampiamente utilizzata per determinare la struttura geometrica e/o elettronica locale della materia basandosi sulla radiazione di sincrotrone per fasci di raggi X intensi e regolabili. Grazie ai protocolli innovativi e alla collaborazione con altri gruppi, il team di Hureau-Sabater ha superato le difficoltà, raggiungendo con successo i propri obiettivi iniziali. «Abbiamo mostrato esattamente perché i farmaci candidati per la AD dovrebbero specificamente bersagliare il rame. Abbiamo testato varie molecole nelle soluzioni e alcune molecole nelle cellule con risultati promettenti». Ciò ha fornito un punto di partenza per gli studi futuri sul potenziale terapeutico degli agenti chelanti del rame (agenti sequestranti) e dei composti correlati. Lungo il percorso, i ricercatori hanno anche messo in evidenza l’utilità dei profarmaci inorganici al posto del ligando parentale esclusivamente organico e scoperto l’importanza delle percentuali di scambio tra i ligandi Aβ, Cu e Zn nonché quella di bersagliare lo stato Cu+ del rame. Hureau-Sabater conclude: «Molti approcci terapeutici per la AD hanno fallito, tra cui quelli mirati agli ioni metallici. Nel progetto aLzINK abbiamo dimostrato la necessità di considerare molti criteri, di cui abbiamo chiarito le caratteristiche importanti»; aLzINK ha aperto una nuova via a terapie mirate con maggiore precisione per la AD che potrebbero potenziare i benefici riducendo nel contempo al minimo gli inutili effetti collaterali.