Rola miedzi w zachorowalności na chorobę Alzheimera
Chorobę Alzheimera opisano oficjalnie po raz pierwszy w 1906 r., a kilka lat później jej klasyfikacja znalazła się w podręczniku do psychiatrii. Pomimo ponad stu lat badań i zbierania danych klinicznych wciąż nie udzielono odpowiedzi na wiele pytań. Zespół finansowanego ze środków Europejskiej Rady ds. Badań Naukowych (ERBN) projektu aLzINK odpowiedział na jedno z nich, wskazując na istotny cel środków kandydujących do miana leków, które mogłyby zapobiec rozwojowi tej wyniszczającej, zwyrodnieniowej choroby neurologicznej.
Nie wszystkie metale są sobie równe
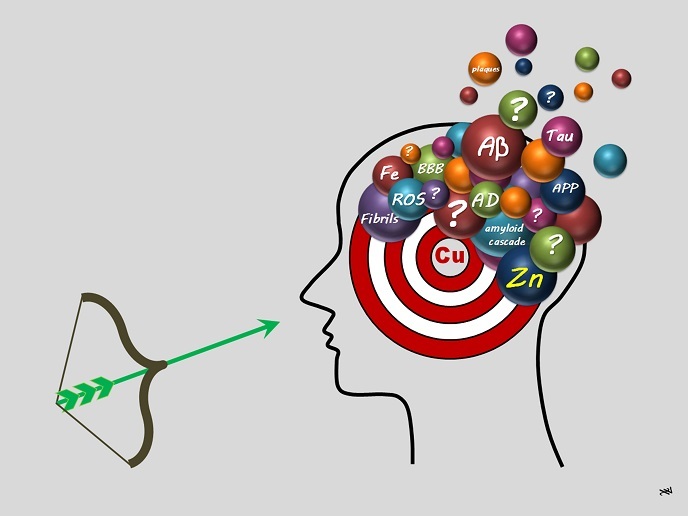
Przez ostatnie 30 lat głównym przedmiotem badań dotyczących choroby Alzheimera była hipoteza kaskady amyloidowej(odnośnik otworzy się w nowym oknie). Zakłada ona, że wczesnym, a zarazem pierwszym kluczowym wydarzeniem w rozwoju tej choroby jest agregacja peptydów beta-amyloidowych(odnośnik otworzy się w nowym oknie) (Aβ) (peptydy składające się z co najmniej dwóch aminokwasów połączonych w łańcuch). Drugim wydarzeniem jest wytwarzanie reaktywnych form tlenu (ang. reactive oxygen species, ROS)(odnośnik otworzy się w nowym oknie) wskutek stresu oksydacyjnego(odnośnik otworzy się w nowym oknie). W końcowym etapie samoczynnie zgrupowane peptydy gromadzą się w tzw. blaszkach starczych, co jest charakterystyczne dla tej choroby. Ze wszystkimi z tych trzech etapów powiązano homeostazę metali (utrzymanie odpowiedniej równowagi metali wymaganej do fizjologicznego funkcjonowania), w szczególności miedzi (Cu) i cynku (Zn). Stypendystka ERBN, Christelle Hureau-Sabater, wyjaśnia: „Miedź może występować w dwóch stopniach utlenienia: Cu+ i Cu2+. Podczas gdy miedź może powodować wytwarzanie ROS, cynk jest chemicznie obojętny i nie ma on takiej możliwości. Oba jony mogą łączyć się z peptydami Aβ, choć w różny sposób, tym samym modulując agregację peptydów Aβ w odmienny sposób. Jedna ze strategii terapeutycznych polega na usuwaniu jonów metali związanych z peptydami Aβ. Wysunęliśmy hipotezę, według której miedź powinna być selektywnie usuwana, co utrudnia tworzenie cząsteczek terapeutycznych/potencjalnych środków leczniczych (zwanych ligandami lub chelatorami)”. Celem projektu aLzINK jest opracowanie wytycznych, w jaki sposób tego dokonać.
Pokonywanie wyzwań, strzał w terapeutyczną dziesiątkę
Peptyd Aβ jest krótkim, inherentnie nieuporządkowanym białkiem składającym się z około 40 aminokwasów, pochodzącym z białka błonowego o dłuższej strukturze. Jego elastyczność i brak wstępnie ukształtowanej struktury przestrzennej utrudniają określenie, w którym miejscu i w jaki sposób miedź i cynk wiążą się z peptydem. Jak mówi Hureau-Sabater, „poradziliśmy sobie z tą trudnością, stosując wiele wzajemnie uzupełniających się technik, w tym skomplikowaną technikę spektroskopii rentgenowskiej(odnośnik otworzy się w nowym oknie)”. Technikę tę powszechnie wykorzystuje się do określania miejscowej geometrycznej i/lub elektronicznej struktury materii w oparciu o promieniowanie synchrotronowe w celu uzyskania intensywnych i możliwych do przestrojenia promieni rentgenowskich. Dzięki innowacyjnym protokołom i współpracy z innymi grupami zespół Hureau-Sabater pokonał wszystkie wyzwania, z powodzeniem realizując swoje założone cele. „Dokładnie wyjaśniliśmy, dlaczego na celowniku środków kandydujących do miana leków na chorobę Alzheimera powinna znaleźć się właśnie miedź. Przeprowadziliśmy testy na różnych cząsteczkach w roztworach i komórkach, w których uzyskaliśmy obiecujące rezultaty”. Stanowi to punkt wyjścia dla przyszłych badań nad potencjałem terapeutycznym chelatorów (czynników chelatujących) miedzi i związków pokrewnych. Przy okazji naukowcy zwrócili również uwagę na użyteczność stosowania nieorganicznych proleków zamiast czysto organicznych ligandów macierzystych i odkryli znaczenie szybkości wymiany pomiędzy ligandami Aβ, miedzią i cynkiem oraz ukierunkowania miedzi na stopień utlenienia Cu+. Hureau-Sabater podsumowuje: „Wiele metod leczenia choroby Alzheimera okazało się nieskuteczne, w tym te ukierunkowane na jony metali. W ramach projektu aLzINK udowodniliśmy, że pod uwagę należy wziąć wiele kryteriów i wyjaśniliśmy ich istotne cechy”. Projekt aLzINK otworzył nowe możliwości w zakresie bardziej precyzyjnych terapii celowanych do leczenia choroby Alzheimera, które mogą zwiększyć korzyści przy jednoczesnym zminimalizowaniu zbędnych skutków ubocznych.