Zusammenhang zwischen Proteinkomplexen, Chromatinstruktur und Krankheiten
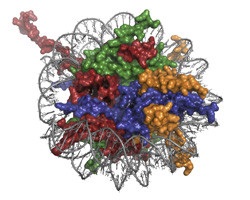
Chromatin ist ein Makromolekülkomplex aus DNA und Proteinen und als solcher an der Regulierung des DNA-Metabolismus (Replikation, Transkription und Reparatur) beteiligt. Die Prozesse werden gesteuert, indem Proteinkomplexe in Wechselwirkung mit strukturellen Untereinheiten des Chromatins treten, so genannten Nukleosomen. Das Projekt MSL1-MSL3-MOF widmete sich nun einem dieser Regulierungskomplexe genauer. Das MOF-Protein ist eine Acetyltransferase und an der DNA-Transkription beteiligt. MSL1 und MSL3 - die beiden anderen Proteine des Komplexes - sind dafür zuständig, die enzymatische Aktivität von MOF zu verstärken. Da noch kaum erforscht ist, wie die Komponenten miteinander und mit dem Chromatin interagieren, sollte die Wissenslücke im Rahmen dieser Studie geschlossen werden. Nach Rekonstitution, Aufreinigung und biochemischer Charakterisierung des Proteinkomplexes wurde eine Karte der Wechselwirkungen zwischen den Komponenten erstellt, um die katalytische Aktivität des Komplexes zu ermitteln. Der Regulierungskomplex wurde dann in einem ersten 3D-Modell rekonstruiert und ein Protokoll für die Assemblierung und Aufreinigung des Chromatinsubstrats entwickelt und getestet. Für röntgenkristallographische Analysen am MSL1-MSL3-MOF-Komplex wurden zunächst am Modellsystem die Kristallisationsbedingungen geklärt und Strukturanalysen durchgeführt. Da kristallographische Analysen bei großen DNA-Protein-Komplexen meist schwierig sind, wurden die Bedingungen an der gut beschriebenen BAH-Domäne (bromo-adjacent homology) definiert, einem Nukleosom-bindenden Protein. Die aufgelöste BAH-Struktur enthüllte eine durch N-terminale Acetylierung induzierte Konformationsänderung, die als posttranslationale Modifikation bei Eukaryoten häufig vorkommt. Die neue Konformationsänderung positionierte acetyliertes BAH näher an das Nukleosom als nicht-acetyliertes BAH, was einen generellen Einfluss der N-Acetylierung auf Proteininteraktionen nahe legt. So konnten mit dem Modellsystem nicht nur die Bedingungen für röntgenkristallographische Analysen des MOF-Komplexes definiert, sondern auch neue Strukturinformationen gewonnen werden. Da viele für die Chromatinregulierung zuständige Proteinkomplexe mit Krankheiten assoziiert werden, könnten Strukturinformationen über diese Proteine zielgerichtete medikamentöse Strategien beschleunigen. Das Projekt war hierzu nun ein erster wichtiger Schritt.