Badanie mechanizmów endocytozy
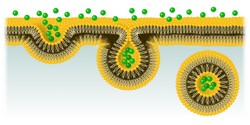
Błona komórkowa stanowi granicę między komórkami i ich mikrośrodowiskiem. Jako taka odpowiada ona za szereg istotnych procesów, takich jak komunikacja między komórkami, przyłączenie do macierzy pozakomórkowej i ruch. Do przyswajania składników odżywczych i cząsteczek sygnałowych komórki wykorzystują wyspecjalizowaną drogę wchłaniania i transportu, znaną jako endocytoza klatryno-zależna (CME). Choć deregulacja CME wiąże się z różnymi chorobami, mechanizm regulujący ten proces jest wciąż słabo poznany. Naukowcy z finansowanego przez UE projektu CME-REG pracowali nad rozszyfrowaniem mechanizmu uruchamiającego ten proces, koncentrując się na kluczowych składnikach: lipidach błony komórkowej, transportowanym ładunku oraz białkach adaptorowych. „Naszym celem było przeanalizowanie etapów endocytozy i wskazanie kluczowych czynników regulacyjnych, które mogą być również powiązane z niektórymi chorobami kojarzonymi z zaburzeniami sygnalizacji komórkowej”, wyjaśnia koordynator projektu dr Zuzana Kadlecova. Regulacja CME Podczas CME składniki odżywcze lub makrocząsteczki przedostające się do komórki wiążą się z receptorami na określonych obszarach zewnętrznej części błony komórkowej. Następujące po tym wchłonięcie ma miejsce w małych pęcherzykach pokrytych z zewnątrz białkiem – klatryną. Obrazowanie żywych komórek pokazuje, że proces CME rozpoczyna się od lokalizacji klatryny i innych białek adaptorowych na cytoplazmatycznej powierzchni błony w jamkach klatrynowych. Aby uchwycić i przeanalizować dynamikę procesu CME, naukowcy opracowali procedurę wykorzystującą ilościowe fluorescencyjne obrazowanie błony podstawnej żywych komórek do obserwacji komórek, w których występują niewielkie zmiany sekwencji głównego białka endocytarnego, AP2. AP2 jest jednym z najbardziej ewolucyjnie konserwatywnych białek, występujących u różnych organizmów, od drożdży do człowieka. Wcześniejsze badania biochemiczne wykazały, że kompleksy AP2 pełnią istotną rolę w inicjowaniu tworzenia jamek klatrynowych. Co ciekawe, AP2 może błyskawicznie zmieniać kształt, jednocześnie zmieniając swoją funkcję i lokalizację. Jednak hierarchia etapów związanych z przejściem AP2 w tryb aktywny, w którym jest gotowe do działania i przechwytywania ładunków, pozostawała dotychczas niejasna. Dzięki mikroskopowym analizom żywych komórek naukowcy mogli zwizualizować tysiące jamek klatrynowych na raz. Wykorzystano również zaawansowane algorytmy śledzenia cząstek i analizy matematyczne, aby zbadać etapy CME i sekwencyjne zmiany konformacyjne, które aktywują AP2 w celu zainicjowania i ustabilizowania procesu tworzenia się jamek klatrynowych. Zespół odkrył, że wiązanie transportowanych ładunków z AP2 jest absolutnie konieczne do stabilizacji powiększającej się w błonie plazmatycznej jamki oraz jej dojrzewania. Komórki z mutacjami w określonych podjednostkach AP2 wykazywały istotnie mniejszą polimeryzację klatryny w miejscach, w których znajdują się jamki klatrynowe, co wyraźnie podkreśla znaczenie określonych miejsc wiązania dla aktywacji AP2. Wyniki badań przeprowadzonych w projekcie CME-REG jednoznacznie potwierdzają poprawność modelu zmian konformacyjnych AP2, w którym białko zmienia swój stan z zamkniętego, niedostępnego dla ładunku, w otwarty, aktywny stan konformacyjny. Rezultaty projektu pokazują, że zmiany konformacyjne są napędzane przez regulację AP2, która odpowiada też za stabilizację nowych jamek klatrynowych. Znaczenie wyników badania Dzięki wysoce interdyscyplinarnemu podejściu naukowcom z projektu CME-REG udało się rozszyfrować mechanizmy molekularne leżące u podstaw regulacji wczesnych etapów CME. Dr Kadlecova pokazała w czasie rzeczywistym, w jaki sposób AP2 kieruje wyborem ładunku do wchłonięcia oraz dokładnie przeanalizowała jego rolę w tworzeniu jamek klatrynowych na wszystkich etapach tego procesu. Chociaż badania prowadzone były na poziomie komórek, najprawdopodobniej można dokonać ich ekstrapolacji do sytuacji in vivo. Biorąc pod uwagę fundamentalne znaczenie AP2 dla prawidłowego rozwoju embrionalnego, wyniki omawianego badania dostarczają również fundamentalnej wiedzy na temat zdarzeń zachodzących na wczesnych etapach życia. Co ważne, pomagają też zrozumieć molekularną etiologię wielu chorób związanych z zaburzeniami endocytozy.