Bessere Wirksamkeit natürlicher Killerzellen für die Krebstherapie
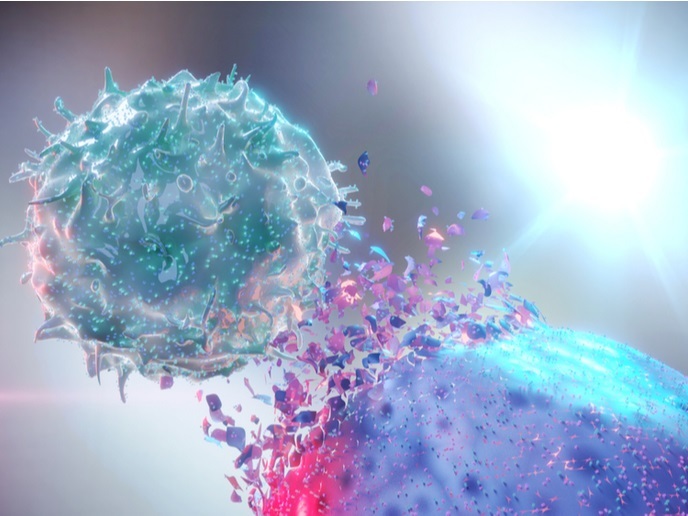
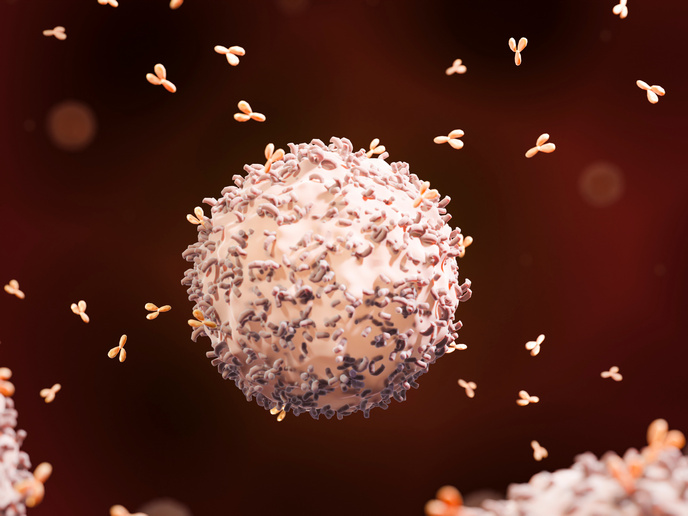
NK-Zellen zeigen direkte zytotoxische Wirkung und kontrollieren nachgewiesenermaßen die Ausbreitung von Krebszellen. Dieser Mechanismus, bei dem NK-Zellen antikörperbeladene Zellen angreifen, wird als antikörperabhängige zellvermittelte Zytotoxizität(öffnet in neuem Fenster) bezeichnet. Doch Tumore haben Abwehrmechanismen, die Überleben und/oder Funktionalität der NK-Zellen vermindern, sodass eine Immuntherapie auf Basis von NK-Zellen bei der Krebsbehandlung noch nicht eingesetzt werden kann.
Funktion und Überleben der NK-Zellen sichern
Auf der Suche nach Strategien zur Verbesserung der Abwehrreaktion auf Tumore und zur Verringerung der Erschöpfung der NK-Zellen hat ein Forschungsteam des Projekts CINK Mechanismen betrachtet, über die die Aktivierung der NK-Zellen gesteuert wird. Die Forschungsarbeiten wurden im Rahmen der Marie-Skłodowska-Curie-Maßnahmen gefördert und befassten sich hauptsächlich mit Strategien, die stimulierende und/oder hemmende Signale kombinieren. „Wir haben eine Vielzahl von Strategien evaluiert, um einen besseren adoptiven Zelltransfer von NK-Zellen als Anti-Krebs-Strategie ermöglichen zu können“, so Pedro Berraondo, Teamleiter am CIMA an der Universität Navarra(öffnet in neuem Fenster), die als Projektträger fungierte. Die Marie-Skłodowska-Curie-Forschungsstipendiatin Maite Álvarez verfolgte unter anderem eine Strategie, bei der die Mechanismen der Immuncheckpoints gehemmt werden und deren Wirkung auf die Funktion der NK-Zellen bewertet wird. An einem dieser Mechanismen sind der PD-1-Rezeptor (engl. Programmed cell death protein 1), der auf der Oberfläche der aktivierten T-Zellen und Liganden exprimiert wird, sowie PD-L1 und PD-L2 beteiligt, die auf der Oberfläche dendritischer Zellen oder Makrophagen exprimiert werden. Unter physiologischen Bedingungen dient deren Interaktion als parallel wirkendes hemmendes Signal zur Verringerung der T-Zell-Antworten und zur Verhinderung einer autoimmunen Entzündung. Doch Tumorzellen überexprimieren PD-L1 und deaktivieren die in den Tumor vordringenden T-Zellen unmittelbar, sodass sie der Zerstörung durch die T-Zellen entkommen. Das Team von CINK hat PD-1 oder PD-L1 mit Antikörpern neutralisiert und dabei eine Verbesserung der Aktivierung und Funktionsweise der NK-Zellen beobachtet, die mit geringerer Erschöpfung einherging. Zudem schuf es eine neuartige Methodik, bei der mithilfe einer Kombination aus Interleukin-15 und Apolipoprotein A1(öffnet in neuem Fenster) aktivierte NK-Zellen erweitert werden können. Diese Strategie wurde umgesetzt und die erzeugten aktivierten NK-Zellen für einen direkten adoptiven Zelltransfer in den Tumor zeigten an Mausmodellen mit Darmkrebs und metastasierendem Melanom vielversprechende Ergebnisse.
Die nächste Etappe für NK-Zellen
Studien zu Krebsimmuntherapien haben verschiedene Komplikationen mit den Ausweichreaktionen von Tumoren, einer immunsuppressiven Mikroumgebung des Tumors sowie einer durch die Behandlung verursachten Toxizität verdeutlicht. Zusammen scheinen sie wirksame und dauerhafte Immunantworten gegen Krebs zu verhindern, sodass die Forschung gezwungen ist, grundlegende Immunkonzepte zu revidieren. Die intrinsischen selbstregulierenden Mechanismen der NK-Zell-Aktivierung haben sich als komplexer herausgestellt als ursprünglich angenommen, wobei sich häufig ein Erschöpfungsphänotyp ausprägt. Das wissenschaftliche Team von CINK hat die Biologie der NK-Zellen erforscht und verschiedene Möglichkeiten untersucht, um eine stärkere und länger anhaltende Aktivierung und Funktion von NK-Zellen auszulösen, damit diese Zellen später im adoptiven Transfer genutzt werden können. Die Ergebnisse aus CINK könnten außerdem bei der künstlichen Gestaltung von NK-Zellen nützlich sein, mit denen chimäre Antigenrezeptoren (CAR) gegen Tumorzellen exprimiert werden – ähnlich ihren Gegenstücken, den CAR-T-Zellen(öffnet in neuem Fenster). „CAR-NK-Zellen haben gegenüber CAR-T-Zellen gewisse Vorteile und können darum als zelluläre Wirkstoffe ‚von der Stange‘ eingesetzt werden“, erklärt Berraondo. Dank der spanischen Vereinigung gegen den Krebs, AECC(öffnet in neuem Fenster), die Álvarez mit einem Forschungspreis ausgezeichnet hat, kann die Forschung von CINK weitergeführt werden. Geplant ist unter anderem eine klinische Studie, die den adoptiven Zelltransfer aktivierter NK-Zellen von einer haploidentischen Spenderin bei Brustkrepspatientinnen untersucht, die mit Antikörpern gegen Tumore vorbehandelt werden.