Die Erforschung der MicroRNA-Deregulierung bei CRC-Patienten
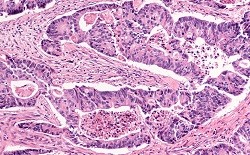
Die Verbindung zwischen MicroRNA-Deregulierung und der Progression von Darmkrebs (CRC) ist bereits bekannt. Doch bei seinem Antrag auf EU-Finanzierung im Jahr 2013 konnte Dr. Valeri nur feststellen, dass die Forscher noch nicht ganz sicher waren, warum und wie diese Deregulierung auftritt: "Auch, wenn mehrere Gruppen eine Verbindung zwischen microRNA-Deregulierung und Darmkrebs identifizieren konnten, wurde die microRNA-Deregulierung noch nicht in Zusammenhang mit wiederkehrenden Anomalien gebracht, die im Frühstadium und beim Fortschreiten von Darmkrebs beobachtet wurden", erinnert er sich. Um diese Wissenslücke zu schließen, befasste sich der Leiter des Teams Gastrointestinal Cancer Biology and Genomics am ICR-Centre for Molecular Pathology die letzten vier Jahre mit zwei wichtigen Fragen. Zuerst beurteilte er, wie genetische und epigenetische Ereignisse zur Kontrolle von microRNA-Genen und Krebs-Phänotypen beitragen. Danach untersuchte er, wie die synthetische letale Interaktion zwischen microRNA-Gen-Aberration und Kinase-Genen dazu beitragen kann, neue Ziele für die Therapie zu definieren. Die Forschung bestand hauptsächlich aus drei Schritten. Dr. Valeri und sein Team begannen mit dem Screening von Fällen von primären und metastasierten Darmkrebsen und griffen dabei auf öffentlich verfügbare Datenbanken und von verschiedenen Institutionen in Europa und den USA gesammelte retrospektive Reihen zurück. Danach führten sie Hochdurchsatz-siRNA- und Arzneimittel-Screenings durch, um Schwachstellen und Wirkmechanismen zu definieren, die mit der MikroRNA-Deregulierung in Verbindung stehen. Schließlich bewerteten sie die Treffer aus ihren Screenings in vitro und in vivo anhand von Darmkrebsmaterial von über 2.500 Patienten. "Alles in allem haben wir die MikroRNA-Deregulierung in gentechnisch veränderten Mausmodellen, in ihren derivativen Organoiden, in menschlichen und Mauszelllinien mit spezifischen Mutationen in Onkogenen sowie in Tumorsuppressorgenen wie APC, KRAS, TP53, PIK3CA und SRC getestet", erklärt Dr. Valeri. "Wir haben auch die MikroRNA-Expression in Geweben von Darmkrebspatienten untersucht, die in klinischen Studien eingeschrieben sind. Und um den Beitrag von spezifischen microRNA in Bezug auf ein anomales Onkogen zu untersuchen, modulierten wir die Expression der microRNA und konnten Veränderungen im Krebsverhalten wie Proliferation, Zelltod, Invasion, Migration und Metastase beobachten." Affektivere Zielbehandlungen entwickeln Mit dieser Forschung konnte das Team nicht nur die wichtigsten MikroRNA identifizieren, die an der Initiation und dem Fortschreiten von Darmkrebs beteiligt waren, sondern auch Hinweise dafür liefern, dass diese als nachgeschaltete Effektoren von Onkogenen und Tumorsuppressorgenen, die bei Darmkrebs häufig mutiert sind, wirken könnten. "Das Targeting und Blocken dieser microRNA könnte zur Entwicklung von neuartigen Therapeutika führen", so Dr. Valeri. Dr. Valeri zeigte auch, dass Mutationen in microRNA-Genen das Ergebnis und die Reaktion auf eine Behandlung bei Patienten mit lokal fortgeschrittenem Rektumkarzinom vorhersagen können. Mit anderen Worten: die Erkennung dieser Anomalien könnte zu einer besseren Auswahl von Patienten und personalisierter Medizin führen. Auf die Frage, wie schnell solche Medikamente kommerzialisiert werden könnten, antwortete Dr. Valeri zurückhaltend. Während MicroRNA-Inhibitoren bereits in klinischen Studien getestet werden, um mehrere Erkrankungen wie chronische Infektionen und Lungenkrebs zu behandeln, werden solche Ansätze in den nächsten Jahren die Validierung in einer frühphasigen klinischen Studie erfordern. In der Zwischenzeit will Dr. Valeri seine Forschungen fortsetzen. "Mithilfe weiterer Fördermittel werde ich den Beitrag von microRNA an kolorektalem und gastroösophagealem Krebs weiter untersuchen. Ich bin zuversichtlich, dass uns dieser Ansatz helfen wird, neuartige therapeutische Ziele und potenzielle Biomarker zu identifizieren, die für die Auswahl von Patienten und die Präzisionsmedizin nützlich sind", schließt er.