Glikany jako kluczowe składniki terapii zwiększających odporność
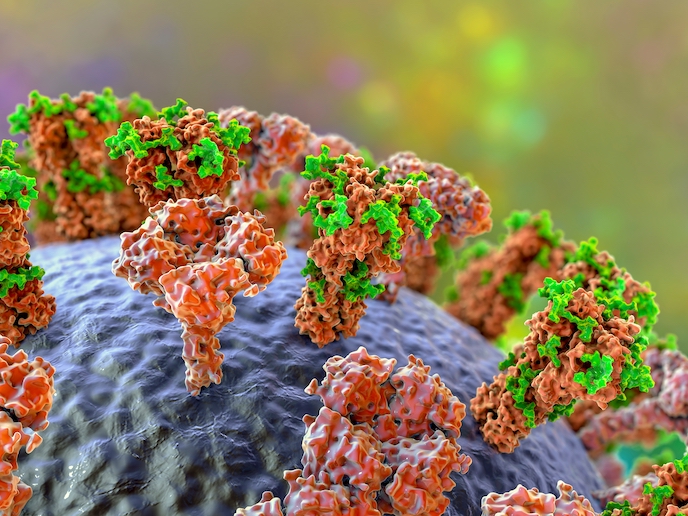
Glikany(odnośnik otworzy się w nowym oknie) to polimery węglowodanowe występujące w dużych ilościach w żywych komórkach. Są kluczowym elementem wielu procesów biologicznych, a ponadto umożliwiają komórkom kierowanie zachodzącymi pomiędzy nimi interakcjami i rozpoznawanie cząsteczek. W obrębie samej komórki glikany biorą udział w składaniu, pozycjonowaniu, transporcie i kontroli jakości białek. Wirusy i bakterie nie dość, że przyczepiają się do glikanów, to białko kolca wirusów, w tym wirusa SARS-CoV-2, może być powleczone glikanami, które działają jak kamuflaż chroniący wirusy przed układem odpornościowym. Zmiany struktury glikanów są nierzadko powiązane z toczącym się w organizmie procesem patologicznym, takim jak stan zapalny lub choroba nowotworowa. Budowa glikanów nie jest zakodowana genetycznie, lecz wynika z działania różnych enzymów przetwarzających glikany, co czyni ich pozycję i skład trudnymi do określenia. Ponadto budowa tych związków jest niezwykle złożona, dlatego wszelkie manipulacje z użyciem dostępnych obecnie metod są trudne. Dlatego zespół finansowanego przez Europejską Radę ds. Badań Naukowych(odnośnik otworzy się w nowym oknie) projektu SWEETOOLS opracował metodologię budowania bibliotek glikanów związanych z peptydem. Te „koniugaty glikopeptydowe” mogą być wykorzystywane do selekcjonowania różnych enzymów przetwarzających glikany. „Wiedza na temat tego, jak konkretne enzymy wiążą się z glikanami i je przetwarzają pozwoli nam odpowiednio dostosować glikopeptydy z naszej biblioteki, tak aby kontrolowały działanie poszczególnych enzymów przetwarzających glikany, torując tym samym drogę do opracowania nowych leków”, wyjaśnia koordynator projektu Milan Vrabel.
Biblioteka glikopeptydów
Zsyntetyzowane biblioteki peptydowe to krótkie łańcuchy aminokwasów – w przypadku biblioteki SWEETOOLS mowa o 4 do 15 resztach – przygotowane przy użyciu metody chemicznej zwanej jedno ziarno jeden związek(odnośnik otworzy się w nowym oknie) (ang. one-bead-one-compound, OBOC). Polega ona na podzieleniu zestawu ziaren żywicy polimerowej zawierających aminokwas na równe porcje i dodaniu do nich kolejnego aminokwasu. Następnie porcje te grupuje się i sprzęga chemicznie z kolejnym aminokwasem. Ziarna po raz kolejny są dzielone, a cała procedura powtarzana. Tak otrzymuje się syntetyczną bibliotekę, w której każde ziarno zawiera unikalną sekwencję aminokwasów, czyli peptyd. Badacze z projektu SWEETOOLS dodali mały inhibitor molekularny, który wiąże się z wybranymi enzymami, otrzymując w ten sposób biblioteki peptydowe zawierające różne aminokwasy, ale taki sam inhibitor. „Peptydy rozpoznają enzymy, dokonują ich selekcji i wiążą się z wybranym enzymem, podczas gdy inhibitor hamuje jego funkcję. Daje nam to możliwość monitorowania wszelkich zmian, w tym, czy zahamowanie funkcji enzymu działa wspomagająco na układ odpornościowy”, dodaje Vrabel. Biblioteka peptydowa powstała dzięki zastosowaniu metod z zakresu chemii „click” – serii szybkich, wydajnych i selektywnych reakcji chemicznych. W kolejnym kroku badacze dodawali do peptydów pozostałość glikanu. Otrzymaną w ten sposób bibliotekę glikopeptydową można wykorzystać do poszukiwania białek, na przykład lektyn, które rozpoznają specyficzne glikany. A ponieważ mechanizm ten wykorzystują również bakterie i wirusy, by związać się z wybranym celem, jego zrozumienie może pomóc skutecznie go osłabiać. Na potrzeby doświadczeń komórkowych badacze opracowali specjalne sondy wytwarzające światło w odpowiedzi na kluczowe reakcje chemiczne, które ułatwiły im śledzenie i szczegółowe obrazowanie biocząsteczek. „Wstępne dane pokazują, że jeden z naszych glikopeptydów chroni limfocyty T przed śmiercią komórkową indukowaną galektyną-1(odnośnik otworzy się w nowym oknie) – mechanizmem, który stosują niektóre komórki rakowe, aby wymknąć się naszemu układowi odpornościowemu. Wykorzystanie tego glikokoniugatu może pomóc w bardziej skutecznej walce z tego typu nowotworami”, przekonuje Vrabel.
„Żywe leki” naszą przyszłością
Zespół odkrył ponadto, że syntetyczne wersje występujących naturalnie glikanów poddawane są przez żywe komórki procesom metabolicznym, dzięki czemu powstają naturalne glikokoniugaty. Zastosowanie metod inżynieryjnych, które umożliwiają „chemiczną” modyfikację glikokoniugatów we wnętrzu lub na powierzchni komórek okazało się skuteczną metodą wytwarzania tańszych immunomodulatorów. „Odczynniki mogłyby pomóc w zatrzymaniu sztucznych cząsteczek na żywych komórkach celem zapewnienia im ochrony, zapobiegając jednocześnie interakcjom komórkowym lub promując nowe interakcje. Moglibyśmy w ten sposób zatrzymywać przeciwciała na komórkach odpornościowych po to, by znajdowały i niszczyły komórki rakowe lub chroniły przed skutkami ubocznymi po przeszczepie narządu”, podsumowuje Vrabel. Zespół projektu złożył już pierwszy wniosek patentowy dotyczący chemicznej re-inżynierii komórkowej, a obecnie planuje rozpoczęcie doświadczeń in vitro z wykorzystaniem różnych linii komórek rakowych.