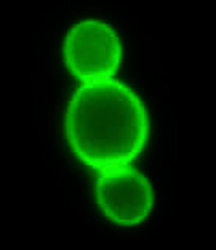
Drożdże pączkujące służą badaniom nad funkcjonowaniem enzymu Gap1
Badania nad wykrywaniem i sygnalizowaniem substancji odżywczych u drożdży stanowią długofalowe przedsięwzięcie, którego realizacją zajmuje się Katolicki Uniwersytet Lowański w Belgii. Są to badania ważne z punktu widzenia zarówno przemysłowego, jak i biomedycznego. Projekt "Yeast sensing" dotychczas skupiał się na badaniu funkcjonowania ogólnej permeazy aminokwasowej (Gap1) u drożdży pączkujących z gatunku Saccharomyces cerevisiae. Białko to jest tzw. transceptorem, ponieważ pełni funkcję zarówno transportera, jak i receptora. Gap1 jest ponadto transporterem aminokwasów działającym także jako bioczujnik aminokwasów przy aktywacji szlaku białkowej kinazy A (PKA) u drożdży. Naukowcy badają związki między aktywacją aminokwasów pośredniczoną przez Gap1 a szlakiem PKA, dążąc do ustalenia elementów na szlaku sygnałowym między Gap1 a PKA. Analiza tych mechanizmów pozwoli zgromadzić nową wiedzę o przesyłaniu sygnału o substancjach odżywczych od transceptora substancji odżywczych do szlaku centralnego regulatora wzrostu będącego pod kontrolą PKA. Jednym z ważnych dotychczasowych osiągnięć jest wydłużenie aktywności trehalazy z około jednej godziny do trzygodzinnego okna. Ponadto po raz pierwszy użyto drożdży w sytuacji, w której warunki umożliwiały trasceptorowi dalszą sygnalizację, gdy uległ już endocytozie. Jednym z niespodziewanych wyników badań jest ukazanie zdolności transceptora Gap1 do podjęcia aminokwasów, a także dwupeptydów niektórych typów. Zespół projektu "Yeast sensing" będzie kontynuować doświadczenia na poziomie molekularnym, aby dokładniej wyjaśnić, jak przebiega sygnalizacja wewnątrzkomórkowa oraz jak jest zatrzymywana w normalnych warunkach. Prowadzone są jeszcze dodatkowe badania, mające na celu ustalenie, czy Npr1 jest substratem dla PKA. To ważne, ponieważ aktywność kinazy Npr1 jest potrzebna do stabilizacji enzymu Gap1 i innych transporterów substancji odżywczych na błonie komórkowej.