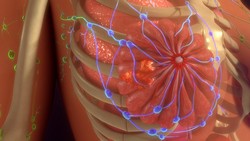
Leczenie przerzutów raka piersi
Jedną z intrygujących cech raka piersi są przerzuty w bardzo wczesnym stadium choroby. Blokowanie potencjału przerzutowego komórek rakowych staje się obiecującym podejściem terapeutycznym. Jak wiadomo, guzy lite charakteryzują się niskim poziomem tlenu – jest to zjawisko zwane hipoksją (niedotlenieniem). Czynnik indukowany hipoksją (HIF) jest głównym czynnikiem transkrypcyjnym odpowiedzialnym za komórkową odpowiedź na bodziec hipoksyczny i przy normalnym poziomie tlenu aktywności HIF zapobiegają enzymy wykrywające tlen – hydroksylazy prolinowe HIF (PHD1-3). Nowe dowody wskazują na to, że przedkliniczna haploinsuficjencja PHD2 w komórkach nowotworowych i stromalnych zmniejszyła przerzuty o 80%. Naukowcy z finansowanego ze środków unijnych projektu PHD2 IN METASTASIS (Dissecting the role of HIF-prolyl-hydroxylase 2 (PHD2) in breast cancer metastasis – identifying novel therapeutic targets) chcieli dowiedzieć się, w jaki sposób blokada PHD2 hamuje rozprzestrzenianie się komórek nowotworowych i przerzutów na poziomie molekularnym. W tym kontekście wykorzystali model spontanicznie rozwijającego się raka piersi, który obejmował wszystkie klinicznie istotne stadia progresji raka piersi. Naukowcy zidentyfikowali dwa podstawowe mechanizmy, które odpowiadają za ograniczenie przerzutów. Zaobserwowali, że PHD2 ma związek z komunikacją parakrynową między komórkami rakowymi a komórkami stromalnymi za pośrednictwem TGF-1β. Wyciszenie PHD2 zmniejszyło aktywację fibroblastów związanych z rakiem (CAF) i przyczyniło się do normalizacji naczyń nowotworowych, co spowodowało zmniejszenie liczby komórek nowotworowych tworzących przerzuty. Fibroblasty CAF wpływają na inwazję komórek rakowych poprzez modulowanie macierzy pozakomórkowej. W innej części projektu naukowcy zbadali terapeutyczne działanie syntazy kwasów tłuszczowych (FAS). Wyniki pokazały, że hamowanie FAS przyczyniło się do zmniejszenia proliferacji komórek śródbłonka i komórek nowotworowych. Dzięki zbadaniu mechanizmu ujawniono, że mechanistyczny cel rapamycyny (ang. mechanistic target of rapamycin, mTOR) został zmodyfikowany po translacji podczas wyciszania FAS, co spowodowało zmniejszenie syntezy białek i ograniczenie proliferacji. Wyniki badania PHD2 IN METASTASIS podkreślają wzajemne oddziaływanie między metabolizmem komórkowym a centralnymi szlakami sygnałowymi, które można wykorzystać do leczenia nowotworów.